二、羰基的保护
1.O,O-缩醛(酮)
2. S,S-缩醛(酮)
醛、酮的保护基相对种类较少,最有效的与常见的保护基团是:无环或有环的O,O-缩醛或缩酮,S,S-缩醛或缩酮以及O,S-缩醛或缩酮等,这和二羟基的保护紧密相联系的;保护基是在酸存在下通过醛或酮化合物与醇、二醇或二硫醇及其衍生物等的反应而引入的;缩醛或缩酮对碱的水溶液或醇溶液,亲核试剂包括有机金属试剂,氢化还原等都是稳定的,能经受较宽的反应条件。

1. O,O-二甲基缩醛(酮)
上保护通式:羰基与醇在质子酸或Lewis酸催化下反应生成O,O-缩醛(酮)

这些衍生物对于还原试剂(如钠-液氨、催化氢化、硼氢化钠及氢化铝锂)、中性和碱性条件下的氧化剂以及格氏等亲核试剂都是稳定的。但它们易被酸水解,甚至用草酸、酒石酸水溶液或酸性离子交换树脂等在温和的条件下都可将其脱除。

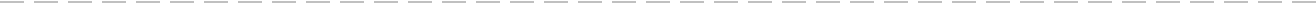
2. O,O-环缩醛(酮)

用于环状缩醛(酮)的二醇保护基:乙二醇及其缩酮、丙二醇及其缩酮,2,2-二甲基-1,3-丙二醇及其缩酮以及芳基取代的二醇衍生物(常使用二醇的环状缩酮作原料来代替二醇进行交换反应)。

常见的二元醇形成环缩醛(酮)的相对反应速率顺序为:

关于O,O-缩醛(酮)保护基的除去,酸催化水解反应是最常用的方法。
需要强调的是,酮的1,3-二氧己环形式缩酮(ketal)比其1,3- 二氧戊环形式的酸催化水解速度快些,而醛的正相反。较之环状缩醛(酮),非环状缩醛(酮)的酸催化水解反应更易进行,也正因它们的不稳定性,其应用受到一定限制。
对于含N原子的缩醛(酮),酸催化水解反应速度相对要慢些,因为酸首先与N原子作用,故常需较强的酸作催化剂。

Lewis酸可在温和条件下去除保护基,如因缩酮的β-位羟基已被TBS保护,酸性条件很易消除TBS,用催化量的PdCl2(MeCN)2处理,可高产率地得到脱保护的产物。

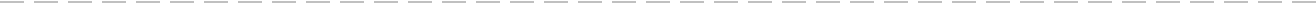
3. S,S-缩醛(酮)
S,S-缩醛(酮)对水解反应的稳定性大(如在O,O-缩醛酮的水解条件下都是稳定的),脱除保护基时使用的条件温和,以及具有反应的高度专一性。
但是多数含硫化合物具有难闻的气味,且脱除该保护基常用到重金属盐,含硫化合物对催化剂Pt和Pd有毒化作用,这时常需用较大量的催化剂和氢高压条件,对氢化还原反应有很大的限制。
S,S-缩醛(酮)保护基的引入:一般用硫醇与羰基化合物在酸催化下反应制得, 由于二硫醇沸点较高(如HSCH2CH2SH的沸点为146-148 ℃,而甲硫醇的沸点仅为34℃ ),因此环状S,S-缩醛(酮)的应用较普遍;常用的二硫醇有1,2-乙二硫醇及1,3-丙二硫醇;质子酸与Lewis酸都可催化这类缩合反应;醛比酮更易于形成S,S-缩醛(酮)。

S,S-缩醛(酮)保护基的脱除
S,S-缩醛(酮)对O,O-缩醛(酮)的水解条件都是非常稳定的,由此可区别这两者,并可作选择性地脱除。较常用 的去除S,S-缩醛(酮)的方法是重金属盐法。

本小结摘录和改编自药物合成反应相关复习资料以及有机崩坏的up笔记,仅作学习交流用途
参考自《药物合成反应》著编译者:孙丽萍,黄文才 科学出版社 2021年01月