实验五 盐酸标准溶液的配制和标定
一、实验目的
1. 掌握减量法准确称取基准物的方法。
2. 掌握滴定操作并学会正确判断滴定终点的方法。
3. 学会配制和标定盐酸标准溶液的方法。
二、实验原理
由于浓盐酸容易挥发,不能用它们来直接配制具有准确浓度的标准溶液,因此,配制HCl标准溶液时,只能先配制成近似浓度的溶液,然后用基准物质标定它们的准确浓度,或者用另一已知准确浓度的标准溶液滴定该溶液,再根据它们的体积比计算该溶液的准确浓度。
标定HCl溶液的基准物质常用的是无水Na2CO3,其反应式如下:
Na2CO3 +2HCl=2NaCl+CO2 +H2O
滴定至反应完全时,溶液pH为3.89,通常选用溴甲酚绿-甲基红混合液或甲基橙作指示剂。
三、仪器及试剂
仪器:25ml酸式滴定管、烧杯、锥形瓶、玻璃棒、250ml容量瓶
试剂:浓盐酸(密度1.19)、无水Na2CO3、甲基橙或者溴甲酚绿-甲基红混合液指示剂:量取30mL溴甲酚绿乙醇溶液(2g/L),加入20mL甲基红乙醇溶液(1g/L),混匀。
四、实验内容
(一)0.1mol·L-1盐酸标准溶液的配制:
量取2.2ml浓盐酸,注入250 mL水中,摇匀。装入试剂瓶中,贴上标签。
(二)盐酸标准溶液的标定:
准确称取0.19~0.21克 于270—300℃灼烧至质量恒定的基准无水碳酸钠,称准至0.0002 g,(至少二份)。溶于50mL水中,加2~3滴甲基橙作指示剂,用配制好的盐酸溶液滴定至溶液由黄色变为橙色,记下盐酸溶液所消耗的体积。同时作空白试验。(空白试验即不加无水碳酸钠的情况下重复上述操作。)
五、数据记录与处理
1.数据记录
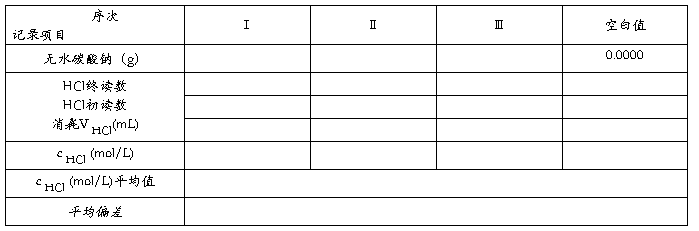
2. 盐酸标准溶液的浓度计算式:
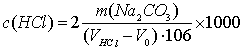
式中:c(HCl)——盐酸标准溶液之物质的量浓度,mol/L;
m——无水碳酸钠之质量,g
V——盐酸溶液之用量,mL
V0——空白试验盐酸溶液之用量,mL
106——无水碳酸钠的摩尔质量,g/ mol。
六、注意事项
1. 干燥至恒重的无水碳酸钠有吸湿性,因此在标定中精密称取基准无水碳酸钠时,宜采用“减量法”称取,并应迅速将称量瓶加盖密闭。
2. 在滴定过程中产生的二氧化碳,使终点变色不够敏锐。因此,在溶液滴定进行至临近终点时,应将溶液加热煮沸或剧烈摇动,以除去二氧化碳,待冷至室温后,再继续滴定。
七、练习题:
1. 在滴定过程中产生的二氧化碳会使终点变色不够敏锐,在溶液滴定进行至临近终点是,应如何处理消除干扰。
2. 当碳酸钠试样从称量瓶转移到锥形瓶的过程中,不小心有少量试样撒出,如仍用它来标定盐酸浓度,将会造成分析结果偏大是偏小。
第二篇:实验六.盐酸浓度的标定
盐酸浓度的标定
一.实验目的
1.学会盐酸溶液的配制和标定 ;
2.掌握滴定操作,并学会正确判断终点 ;
3.熟悉电子天平的使用、减量法称量
二.实验原理:
为什么要滴定?
什么是基准物质?
能够准确滴定的条件
终点的判定(能否滴到第一等当点),指示剂的选择,
酸碱指示剂
计算公式
实验结果的表示(误差、数据处理、真实值、平均值、准确度、精密度、置信水平、数据的取舍等)
1.浓盐酸有挥发性, 因此标准溶液用间接方法配制, 配好的溶液只是近似浓度, 准确的 HCl 浓度需用基准物质进行标定。通常用来标定 HCl 溶液的基准物质有无水碳酸钠 (Na2CO3 )和硼砂( Na2B4O7·l0H2O)。本实验采用无水碳酸钠为基准物质来标定时, 以溴甲酚绿-二甲基黄混合指示剂指示终点, 滴定反应为:
Na2CO3 + 2HCl = 2NaCl + H2O + CO2 ↑
2.⑴计算化学计量点的pH : 在Na2CO3标定盐酸溶液浓度的反应中 :
Na2CO3 + 2HCl = H2CO3(CO2+H2O) + 2NaCl产物H2CO3饱和溶液的浓度约0.04mol·L-1,溶液的pH值为[H+]=(Ka1c)-1/2 =(4.4×10-7×0.04)-1/2 = 1.3×10-4mol·L-1,pH=3.9
⑵混合指示剂变色点的pH : 溴甲酚绿-二甲基黄混合指示剂变色点的pH为3.9,因此与化学计量点的pH值吻合,可选作指示剂。
三.主要仪器与试剂
主要仪器:电子天平,250m烧杯(3个),50mL酸式滴定管,称量瓶
主要试剂:HCl (aq)、无水碳酸钠(s)、溴甲酚绿-二甲基黄混合指示剂
实验操作:
称量瓶的洗涤和干燥(烘箱)
干燥器的使用
减量称量法
滴定
四.操作步骤:
1.盐酸标准溶液浓度的标定:
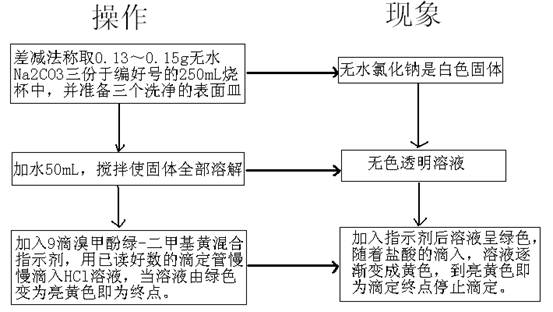
五.数据记录与处理
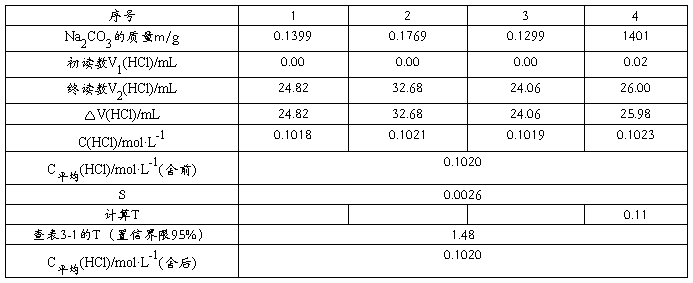
用到的计算公式:
1.盐酸浓度的计算:c(HCl)= 
2.平均值的计算: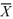 =(X1+X2+X3+……+Xn)/n
=(X1+X2+X3+……+Xn)/n
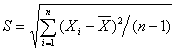 3.标准偏差计算:
3.标准偏差计算:
4:统计量计算式为:Tn=(Xn-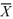 ) / S
) / S
Grubbs检验法P100
六.问题及思考题
★思考题
1.配置0.1mol·L-1盐酸溶液时,用何种量器量取浓盐酸和蒸馏水?
答:由于配制的盐酸溶液浓度是粗略的,因此浓盐酸用量筒量取;纯水也用量筒量取
2.在称量过程中,出现一下情况,对称量结果有无影响,为什么?
1) 用手拿称量瓶或称量瓶的盖子;
2) 不在盛入试样的容器上方,打开或关上称量瓶盖子
3) 从称量瓶中很快倾倒试样;
4) 倒完试样后,很快竖起瓶子,不用盖子轻轻的敲打瓶口,就盖上盖子去称量;
5) 倒出所需质量的试样,要反复多次以至近10次才能完成。
答:以上情况对称量结果都有影响,原因如下:
1) 避免称量瓶沾上脏物,对称量结果造成影响
2) 瓶口沾的试样落在烧杯外而损失。
3) 很快倾斜瓶身会使试样冲出,易倒多;粉末试样会扬起粉尘而损失
4) 很快竖起可能扬起粉尘而损失试样;轻击瓶口,可将沾在瓶口的试样或落入瓶内,或落入烧杯内,避免试样损失。
5) 在称样过程中试样吸水,引进误差。
3. 以下情况对实验结果有无影响,为什么?
1) 烧杯只用自来水冲洗干净;
2) 滴定过程中活塞漏水;
3) 滴定管下端气泡未赶尽;
4) 滴定过程中往烧杯加少量的蒸馏水;
5) 滴定管内壁挂有液滴。
答:有影响的是:1),2),3),5) ;4)无影响。 原因如下
1) 自来水呈酸性,且有较多的杂质,会影响滴定的准确性;
2) 旋塞漏水,则无法知道加入滴定液的准确体积,无法得到终点;
3) 有气泡会影响滴加的酸的准确体积;
4) 少量的蒸馏水不会影响滴定准确性,因为它本身是中性;
但加大量的蒸馏水会影响,因为冲洗了溶液。
5) 管内壁挂液滴,会导致无法知道加入滴定液的准确体积。
★问题:
1.氢氧化钠和盐酸能否作为工作基准试剂?能否直接在容量瓶中配置0.1000mol·L-1的氢氧化钠溶液?
答:不能,氢氧化钠和盐酸都不符合基准试剂的要求;
由于浓盐酸挥发,浓度不确定,因而无法准 确配置成标准溶液,
而NaOH易吸收空气中的水和CO2,其纯度、浓度均不定,也无法配置
0.1000mol·L-1的氢氧化钠标准溶液。
2.能否用酚酞作指示剂标定 HCl溶液,为什么?
答:不能主要是终点由微红色变成无色,人的肉眼很难判断,误差大。
选择指示剂的一般原则是指示剂的理论变色点pK(HIn)处于滴定突跃范围内。因酚酞的pKa=9.1,变色范围为8.2~10.0。酚酞微红时pH=9,此时反应仅进行到HCO3-(CO32- + H+ = HCO3-),因此不能用酚酞作指示剂,指示产物为NaCl+H2CO3的化学计量点(pH=3.9)。
3.草酸钠能否用来标定盐酸溶液?
答:可以。草酸钠符合基准物的标准,也符合酸碱的条件,可以用作指示剂滴定。
不可以,因为草酸的Ka1太大,草酸钠的Kb2太小,不能满足准确滴定的条件。
七.注意事项与讨论:
1.带进天平室的物品:
250mL烧杯编号盖上表面皿(不放玻棒);干燥器;称量瓶与纸带(放干燥器内);记录笔、实验报告本。
1. 减量法称量的注意:
1) 盛有试样的称量瓶除放天平盘、干净的纸或表面皿上,或用纸带拿在手中外,不得放其它地方。
2) 纸带放洁净、干燥的地方;请保存好以便以后再用;
3) 取出或套上纸带时,不要碰到称量瓶口
3.滴定注意:
1) 使用前摇匀盐酸溶液;溶液必须直接倒入滴定管,不经烧怀;
2) 搅拌时玻棒不碰杯壁,不能从烧杯中取出
3) 操纵活塞时手的姿势正确,手心不能顶活塞
4) 从滴定开始直到终点,注意控制不同阶段的滴定速度。通过预先练习,做到自如控制滴加1滴、半滴,以准确掌握终点;
5) 纯水的pH为6左右,终点前洗杯壁、玻棒不要太早,水不宜太多。要用尽量少的水将杯壁洗净
1、0.1mol·L-1盐酸标准溶液的浓度为什么要标定,而不能准确配制;
浓盐酸易挥发,不能作工作基准试剂。
标准物质必须符合哪些条件?
Ø 其组成与化学式完全相符;
Ø 纯度足够高,一般在99.9%以上;
Ø 性质稳定;
Ø 没有副反应;
Ø 摩尔质量比较大
有哪些标准物质可标定盐酸溶液的浓度?
无水碳酸钠:Na2CO3+2HCl=2NaCl+H2O+CO2↑化学计量点的pH=3.89;
硼砂(Na2B4O7·10H2O):Na2B4O7·10H2O+2HCl=4H3BO3+2NaCl+5H2O
化学计量点的pH为5.1;
用NaOH标准溶液。
2、在标定过程中,HCl与Na2CO3发生了哪些反应,有几个化学计量点,计量点的pH各是多少?
Na2CO3+HCl=NaCl+NaHCO3
+) NaHCO3+HCl=NaCl+H2CO3
Na2CO3+2HCl=2NaCl+H2CO3
H2CO3的饱和度约为0.04mol/L,计量点pH约为3.9
3、如何选择指示剂?
酸碱滴定曲线、滴定的突跃范围:强碱滴定强酸时,随着NaOH溶液的加入,溶液pH值发生变化,以pH对NaOH的加入量作图得滴定曲线,计量点前后NaOH溶液由不足到过量0.02mL(0.1%);
溶液pH的突然变化称滴定突跃,突跃的pH范围称滴定突跃范围;
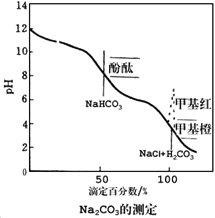
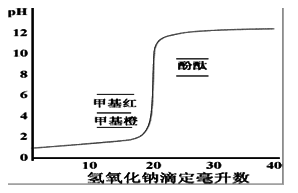
酸碱指示剂、指示剂的变色范围 酸碱指示剂本身是弱酸或弱碱:HIn = H+ + In-,HIn与In-有不同的颜色,pH=pKa(HIn)+lg[In-]/[HIn],当[In-] =[HIn],pH=pKa为理论变色点;[In-]/[HIn]≤ 0.1看到酸色,≥10,看到碱色
变色范围的pH=pKa±1,但实际观测到的与理论计算有差,因人眼对各种颜色的敏感度不同,加上两种颜色互相掩盖,影响观察。如酚酞pKa=9.1,变色pH范围为8.0~9.6。不同的人的观察结果也不同。
指示剂的选择 使指示剂的理论变色点处于滴定突跃范围。Na2CO3标定盐酸的化学计量点的pH=3.9,实验中使用二甲基黄-溴甲酚绿为指示剂,变色点pH=3.9,该指示剂的碱色为绿,酸式为橙,变色点pH时为亮黄色。
4、计算公式。
c(HCl)= 2m(Na2CO3) = 2m(Na2CO3)
V(HCl)*M(Na2CO3) 105.99V(HCl)
⑴差减法称取0.13~0.15g无水Na2CO3四份
怎样确定称取Na2CO3的克数?
Ø 一般滴定液用去的体积为25mL左右,相当的Na2CO3量为:
m=c HCl ? v HCl ? MNa2CO3 /2000
= 0.13(g)
Ø 称量时允许有一定的范围,故称0.13~0.15g。若滴定体积太小,滴定管读数引入的误差较大。如v HCl为10mL,读数误差为2×0.01mL,相对误差为:2×0.01/10 ×100% = 0.2 % 。若为25mL,则相对误差为:2×0.01/25 ×100% = 0.08 %。
带哪些物品进天平室?
Ø 搪瓷托盘
Ø 烧杯编号盖上表面皿(不放玻棒);
Ø 干燥器;
Ø 称量瓶与纸带(放干燥器内);
Ø 将干燥器、烧杯放搪瓷盘内,平端进天平室(为什么);
Ø 记录笔、实验报告本
减量法称量的要点?
Ø 称出称量瓶质量,按去皮键TAR,倾倒试样后称量,所示质量是“—”号;
Ø 再按去皮键称取第二份试样;
Ø 本实验连续称取四份试样。
Ø 注意事项(减量法称量的注意点)
Ø 盛有试样的称量瓶除放天平盘或干燥器内,或用纸带拿在手中外,不得放其它地方(为什么);
Ø 纸带放洁净、干燥的地方;请保存好以便以后再用;
Ø 取出或套上纸带时,不要碰到称量瓶口
Ø 要在承接容器的上方打开(或盖上)瓶盖,以免使粘附在瓶口、瓶盖上的试样失落在容器外,粘在瓶口的试样应尽量敲入烧杯或称量瓶内;
Ø 在烧杯上方,边敲边倒,边敲边竖
Ø 若倒入试样量不够时可重复再倒,但要求2~3次内倒至规定量(为什么)。如倒入量大大超过,弃去,洗净烧杯后重称。
(2)溶解试样 加水50mL,搅拌使固体全部溶解
1、 怎样溶解试样?
答:⑴取下表面皿,用洗瓶吹洗烧杯壁,将杯壁上可能有的粉末试样洗至杯底,放入玻棒。
⑵用量筒取50mL纯水,沿玻棒(玻棒下端要靠杯壁)或沿杯壁缓缓加入到烧杯中。现烧杯上均有容量刻度,但体积数不准,不要使用。
⑶用玻棒不断搅拌使所有的固体溶解,但不碰杯壁以免发出响声。注意已放入的玻棒不能离开烧杯,更不能放在烧杯以外的地方,以免烧杯中的试样损失。
2、 为何要将试样完全溶解?
答:如试样未完全溶解,在后续滴定步骤中,会导致只有部分试样与盐酸反应,使盐酸体积偏小,浓度偏高,准确度差。还会造成平行测定的实验结果精密度差。
 注意事项
注意事项
Ø 量筒量取纯水,沿杯壁加入,或玻棒引入,玻棒下端紧靠杯壁;每只烧杯内放一根玻棒,放入后不再取出;
Ø 搅拌时不碰杯壁以免发出响声;
Ø 试样完全溶解后再滴定,重做时更要做到此点。
(3)滴定
加入9滴溴甲酚绿-二甲基黄混合指示剂,用已读好数的滴定管慢慢滴入HCl溶液,当溶液由绿色变为亮黄色即为终点。
3、 为什么选用溴甲酚绿-二甲基黄混合指示剂作标定反应的指示剂?
答:⑴计算化学计量点的pH :
在Na2CO3标定盐酸溶液浓度的反应中 : Na2CO3 + 2HCl = H2CO3(CO2+H2O) + 2NaCl产物H2CO3饱和溶液的浓度约为0.04mol·L-1,溶液的pH值为[H+]=(Ka1c)-1/2 =(4.4×10-7×0.04)-1/2 = 1.3×10-4mol·L-1 pH=3.9
⑵混合指示剂变色点的pH :
溴甲酚绿-二甲基黄混合指示剂变色点的pH为3.9,因此与化学计量点的pH值吻合,可选作指示剂。
4、 混合指示剂在滴定过程中颜色如何变化?
答: 混合指示剂在不同pH值时颜色的变化 :
二甲基红:pH=4.0 黄色,PH=2.9 红色
溴甲酚绿:PH=5.4 蓝色,PH=3.8 黄色
二甲基红+溴甲酚绿: PH=3.9
绿色(黄色+蓝色) 黄色 橙色(红色+黄色)
由以上分析,可知在Na2CO3溶液中,混合指示剂显蓝绿色,随着HCl的加入蓝色成份减少 → 绿 → 黄绿(终点前)→ 亮黄(终点) → 橙色(过终点)。
5、 标定盐酸溶液浓度时能否用酚酞作指示剂?
答: 选择指示剂的一般原则是指示剂的理论变色点pK(HIn)处于滴定突跃范围内。因酚酞的pKa=9.1,变色范围为8.2~10.0。酚酞微红时pH=9,此时反应仅进行到HCO3-(CO32- + H+ = HCO3-),因此不能用酚酞作指示剂,指示产物为NaCl+H2CO3的化学计量点(pH=3.9)。
6、 滴定过程中,如何控制好滴定的速度?
答: ⑴滴定开始时,可快。由于离终点远,滴落点颜色无明显变化,此时的滴定速度为10mL/min,即每秒3~4滴,呈“见滴成线”,但不能成“水线”,以免溶液溅出。
⑵滴落点颜色有变化或消失慢时,滴定放慢。随着终点的接近,改为滴1滴搅几下(一滴多搅),或控制滴加速度为加1滴,经搅拌后溶液颜色稳定,下1滴正好滴下。
⑶近终点 :先洗玻棒、杯壁,微移旋塞,使溶液悬在下口形成半滴,用玻棒下端靠下(注意玻棒只能接触液滴,不要接触管尖),快速搅动溶液。
7、 为什么近终点时要洗杯壁,洗涤水的量要不要控制?
答: ⑴滴定过程中,可能有溶液溅在杯壁,因此近终点时要洗杯壁。
⑵只能用少量水洗杯壁。在盐酸标准溶液的标定中,变色点pH=3.9,因纯水pH=6,多加洗涤水,会多消耗盐酸,从而引进误差。因此终点时加少量纯水,对终点没有影响;加多了不行。
8、 近终点时应注意什么?
答:⑴近终点时应加速搅动溶液,促使CO2逸出。因反应产物是
H2CO3(CO2+H2O),在室温下易形成CO2的过饱和溶液,使溶液的酸度稍稍增大,终点稍稍提前。
⑵终点的颜色是亮黄色,如黄中带绿的成分,说明终点未到;如黄中带橙呈金黄,则终点已稍过。为了掌握终点的亮黄色,可在测定前,取Na2CO3固体配成溶液后练习终点的判断,练习加1滴、半滴的操作。
⑶如对终点颜色的判断无把握,可在确定第一份终点后,请指导教师指导。也可通过对比摸索,先读好数,记录(在报告纸反面),根据需要,在滴定管下口悬1滴或半滴,靠下,搅动溶液、观察颜色,记录。如还不能确定,可再重复,在对比中确认终点后,读数即确定,记录在表格,请指导教师批阅。
 注意事项
注意事项
Ø 使用前摇匀盐酸溶液;溶液必须直接倒入滴定管,不经烧怀;
Ø 搅拌时玻棒不碰杯壁,不能从烧杯中取出;
Ø 操纵活塞时手的姿势正确,手心不能顶活塞
Ø 从滴定开始直到终点,注意控制不同阶段的滴定速度。通过预先练习,做到自如控制滴加1滴、半滴,以准确掌握终点;
 纯水的pH为6左右,终点前洗杯壁、玻棒不要太早,水不宜太多。要用尽量少的水将杯壁洗净(为什么);
纯水的pH为6左右,终点前洗杯壁、玻棒不要太早,水不宜太多。要用尽量少的水将杯壁洗净(为什么);
Ø 标定测四份。每份滴定结束后,滴定管中必须加液至零刻度附近,再进行下一次的滴定(为什么)。
教学安排
 先洗称量瓶,放进烘箱后开始讲课;
先洗称量瓶,放进烘箱后开始讲课;
 课堂讨论结束后,取出称量瓶,检查瓶内有无水;已烘干的称量瓶放干燥器中冷却(20分钟)、待用;
课堂讨论结束后,取出称量瓶,检查瓶内有无水;已烘干的称量瓶放干燥器中冷却(20分钟)、待用;
 准备好大、小纸带 ;
准备好大、小纸带 ;
 先称量、溶样,后准备滴定管滴定
先称量、溶样,后准备滴定管滴定
扩展实验:混合碱的测定
实验步骤

数据记录与处理
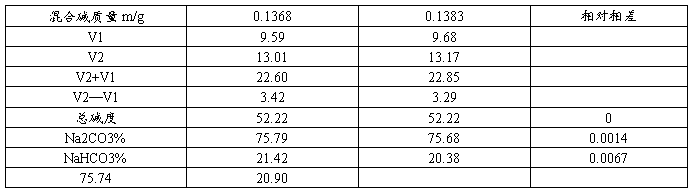
由相对相差<3%,则测定结果合理。
计算公式
1.先根据V2—V1与V1的关系得出混合碱的组成,V2—V1<V1,则组成为NaOH和Na2CO3
V2—V1>V1,则组成为Na2CO3和NaHCO3
2. 当V2> V1时:
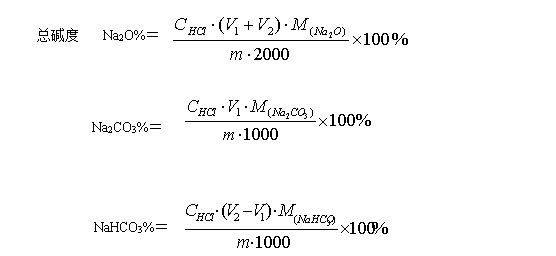
3.当V1> V2时
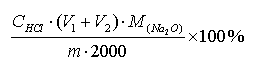
总碱度Na2O%=
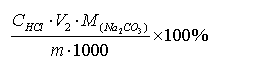
Na2CO3%=
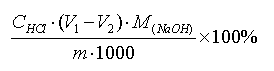
NaOH%=
