第一个发现的细胞内第二信号——cAMP信号通路(下)
“和周老师一起学KEGG通路”系列持续更新中,继上一期周老师分享过cAMP通路的简介以及在kegg通路中的位置、cAMP通路的简要结构、cAMP直接调节的下游通路(文章链接:《第一个发现的细胞内第二信号——cAMP信号通路(上) 》 ),本期将继续介绍PKA蛋白以及调节的下游通路,更有基迪奥客户相关经典文献解析,一起来看看吧。
PKA蛋白以及调节的下游通路
PKA激酶的构成以及与cAPM的调控关系
cAMP通路又叫做PKA通路,因为PKA是cAMP最重要的下游靶蛋白。PKA是cAMP依赖的蛋白激酶(cyclic-AMP dependent protein kinase A),一般认为, 真核细胞内大部分cAMP的作用都是通过活化PKA,从而使其底物蛋白发生磷酸化而实现的。
PKA全酶分子是由四个亚基组成的四聚体,其中两个是调节亚基(regulatory subunit, 简称R亚基),另两个是催化亚基(catalytic subunit, 简称C亚基)。在大多数哺乳类细胞中,至少有两类蛋白激酶A,一类存在于胞质溶胶(I型), 另一类结合在质膜、核膜和微管上(II型)。
PKA全酶没有活性,在没有cAMP时,以钝化复合体形式存在。cAMP与调节亚基结合,改变调节亚基构象,使调节亚基和催化亚基解离,释放出催化亚基。活化的蛋白激酶A催化亚基可使细胞内某些蛋白的丝氨酸或苏氨酸残基磷酸化,于是改变这些蛋白的活性,进一步影响到相关基因的表达。
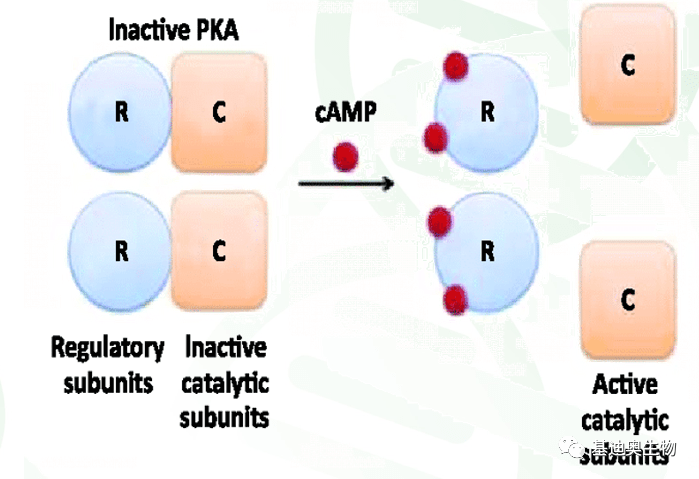
图1 PKA全酶构成以及被cAMP解离活化的过程
如果你在GeneCards数据库搜索“PKA”,那么会得到以下的结果。一共涉及7个基因,包括三个PKA催化亚基基因(PRKACA、PRKACB、PRKACG)和4个PKA调节亚基基因(PRKAR1A/B,PRKAR2A/B)。
图2 在GeneCards数据库中搜索PKA的结果
在kegg数据库中没有提到的一点是PKA通过一种叫做AKAPs (A-激酶锚定蛋白)的骨架蛋白定位在特定的细胞位置上。 通过这个骨架蛋白,PKA、相关其他调控蛋白和PKA底物可以聚集在一起,并由cAMP激活对底物的磷酸化效应。AKAP同样是一个蛋白家族,在人体内有10多个拷贝,其异常会导致PKA下游通路异常导致疾病。
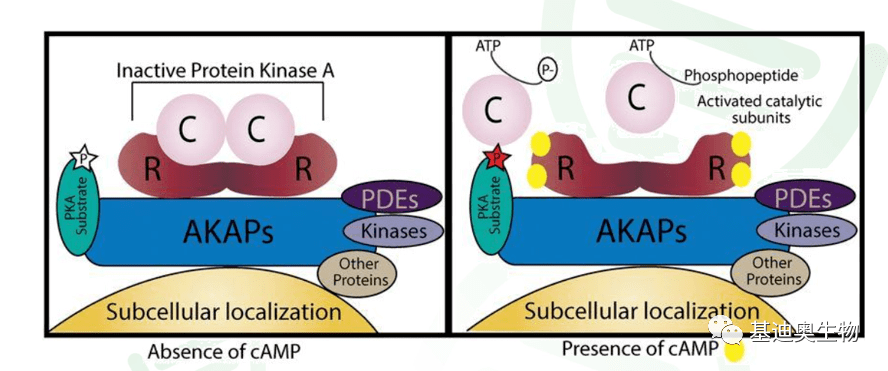
图3 AKAP作为结构蛋白可以调节PKA的细胞定位以及磷酸化作用
另外,cAMP、PKA与PDE之间也会形成闭环的负反馈机制。如下图,cAMP激活PKA的催化活性后,PKA却会激活PDE,从而水解cAMP。这个负反馈机制自动形成了“刹车”系统,从而保证细胞不会持续处于cAMP信号激活的状态。
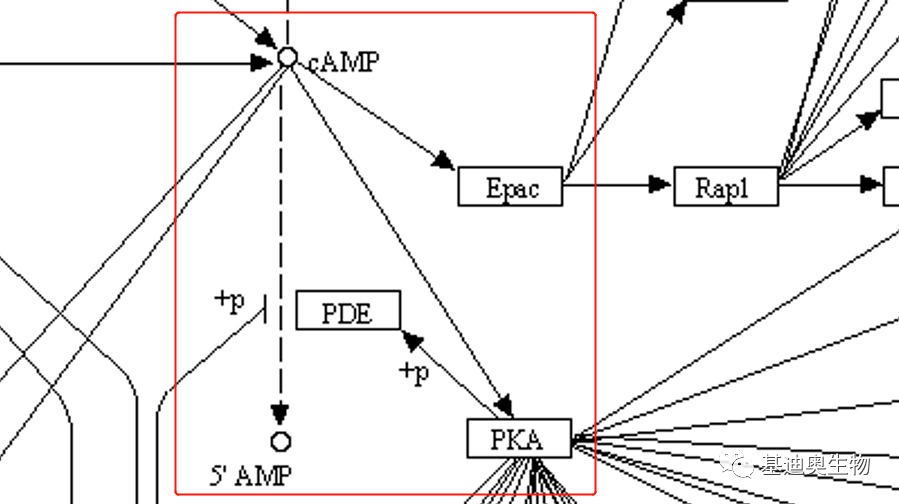
图4 cMAP-PKA-PDE的负反馈环
PKA激酶的靶蛋白以及下游通路
蛋白激酶PKA激活的下游通路十分丰富,但可以从3个维度进行分类:
①调节转录调控
PKA直接或者间接活化转录因子,从而激活下游转录。对应在kegg图中,粗虚线是细胞核膜,呈现了下游转录因子对DNA转录的调控作用。图中呈现了若干种组织/细胞中的PKA调控作用。
在海马神经元(Hippocampal neuron)中,PKA可以通过Rap1激活的MAPK途径间接激活或者直接激活转录因子CREB(cAMP-response element binding protein,环磷腺苷效应元件结合蛋白),启动转录的下游基因包括BDNF、fos、jun。
其中BDNF在发育过程中,促进外周和中枢神经系统的选定神经元群体的存活和分化,参与轴突生长、寻路以及树突生长和形态的调节。而FOS则可以与JUN家族蛋白质二聚化,形成转录因子复合物AP-1,然后调控海马神经元的超兴奋性、细胞的死亡/存活。
在胚胎成纤维细胞(embryonic fibroblast)中,PKA通过磷酸化抑制GLI3的转录因子活性,从而抑制刺猬通路(Hedgehog signal pathway)的信号。
在青春期前(prepubertal)的睾丸支持细胞(sertoli cell)里,PKA则可以通过激活明星转录因子IkB、NFKB、SOX9,来增加抗苗勒管激素(AMH)的分泌。
在肝细胞(hepatocyte)中,PKA通过活化PPARα,来增加酰基辅酶A氧化酶ACO的编导,从而促进脂肪酸的β氧化。
在血管平滑肌细胞里,PKA则可以通过磷酸化抑制NF-AT的转录活性,降低PAR1(凝血因子ⅱ凝血酶受体)的表达,从而调节血栓形成反应。
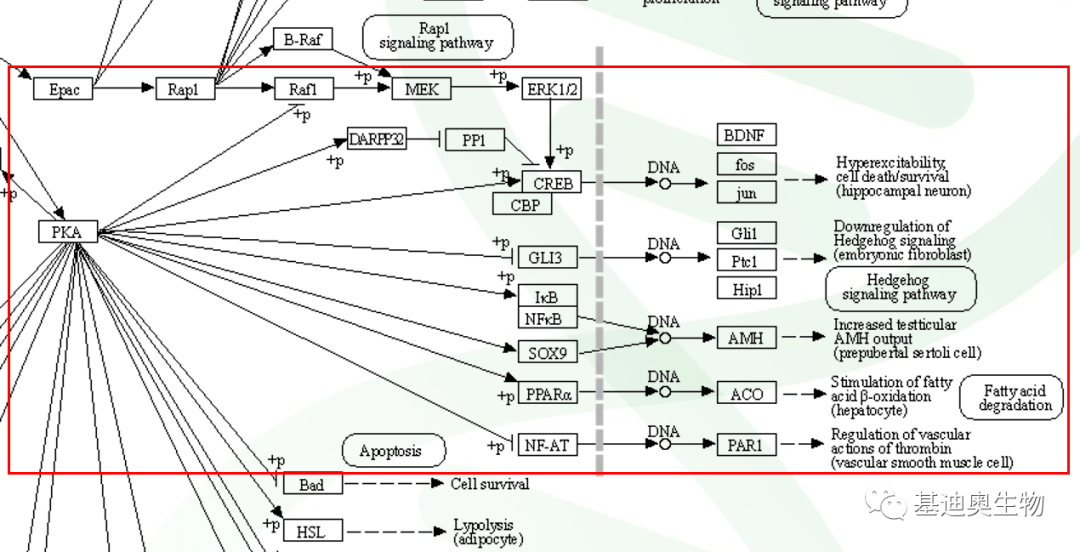
图5 PKA调节的下游转录调控
②细胞生理生化调节
Kegg图这个部分展示了PKA下游非转录因子途径对生病生理生化状态的调节。
PKA具有抑制细胞凋亡的作用。在PI3K-AKT通路,我们提起过BAD具有促凋亡的作用。而PKA对BAD的磷酸化,则可以抑制BAD的促凋亡活性。
在白色脂肪组织的脂肪细胞(Adipocyte)中,PKA可以活化脂肪酶E(HSL),促进将储存的甘油三酯水解为游离脂肪酸,发挥脂类分解作用(Lypolysis)。这是脂肪细胞释放储存的能量的主要途径。
在内皮细胞(endothelia cell)和平滑细胞中,PKA可以抑制小G蛋白Rho(RHOA), 从而最终调节肌球蛋白MLC,来松弛肌细胞。
在心肌细胞中(cardiac myocyt),PKA可以通过调节肌钙蛋白(TnI)和心脏磷蛋白(PLB)来调节心肌细胞Lusitropy( 松弛)和Inotropy( 收缩)。kegg图中,就展示了在心肌细胞的肌质网(sarcoplasmic reticulum)内,PKA通过蛋白磷酸化, 如与肌浆网 Ca2+ 转运有关的收缩蛋白受磷蛋白(PLB)及Ca2+ 通道蛋白(RyR2)等的磷酸化,可加速离子的跨膜转运,缩短动作电位时程,增强心肌舒缩功能,从而维持心肌的正常节律。
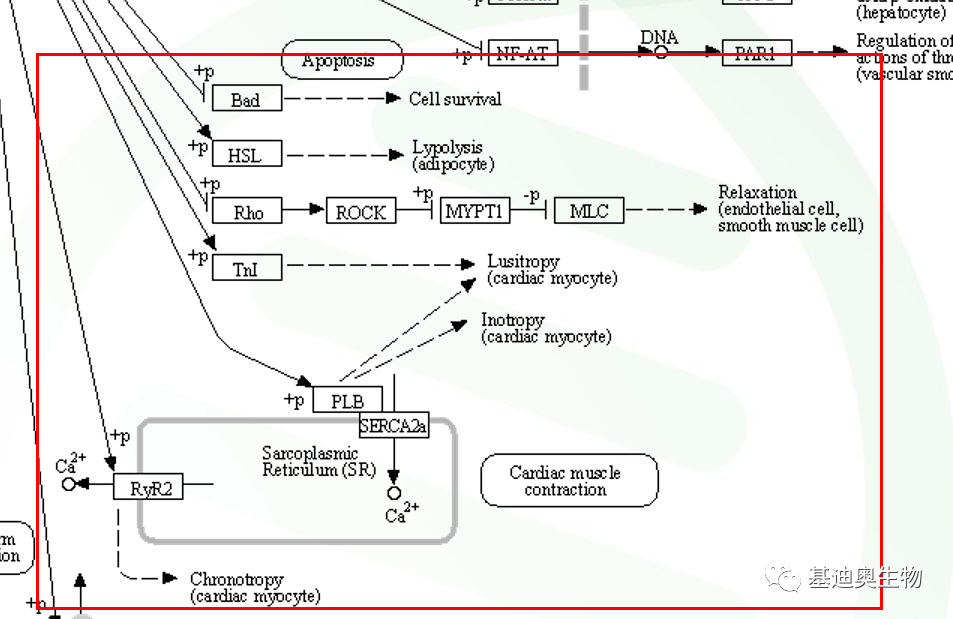
图6
③调节细胞膜跨膜离子转运
PKA还可以直接通过对细胞膜上的通道蛋白、转运蛋白以及受体的磷酸化,调节钙、钾、钠、氯等离子的跨膜转运,从而调节胰腺分泌(pancreatic secretion)、胆分泌(bile secretion)以及中枢神经系统的长时程增强作用(long-term potentiation)。
其中涉及的通道蛋白、转运蛋白以及受体蛋白包括:钙电压门控通道蛋白(VDCC),ATP酶质膜 Ca2+ 转运蛋白(PMC),钙释放激活钙通道蛋白(SOC/ ORAI),ATP酶钠钾离子转运蛋白, 氯离子通道蛋白(CFTR),离子型谷氨酸受体AMPAR和NMDAR。
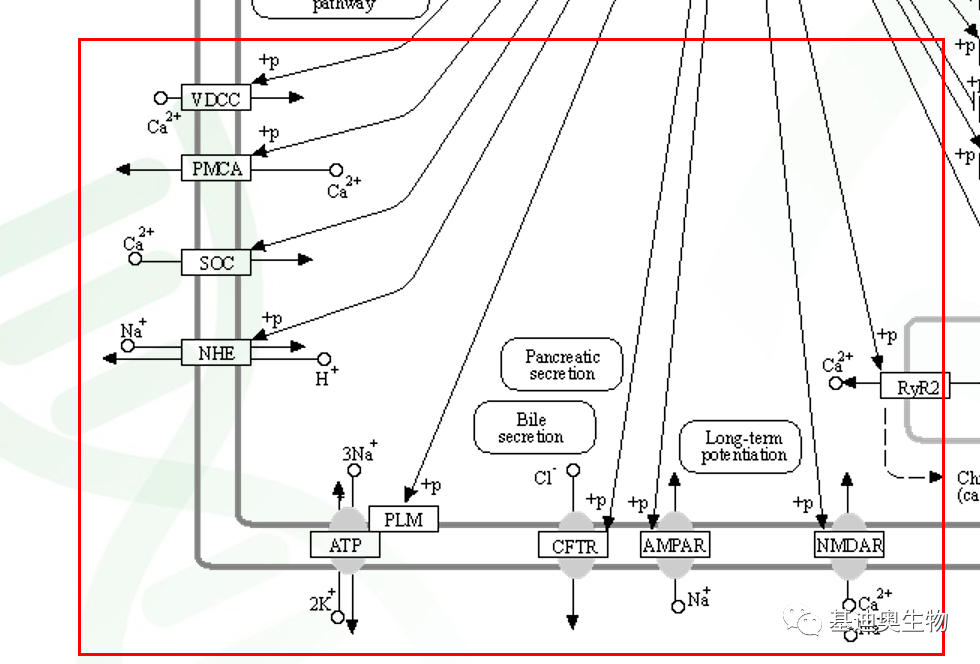
图7
从上文介绍,我们可以看出cAMP通路在各类组织、各类细胞中起着非常广泛的作用,在很多文章中我们可以看到这个通路的身影。基迪奥合作客户2019年的发表在cell的单细胞测序文章《Mucosal Profiling of Pediatric-Onset Colitis and IBD Reveals Common Pathogenics and Therapeutic Pathways》就重点提及了cAMP通路。
这篇文章的背景:儿童期发病的结肠炎(Pediatric-onset colitis)和儿童炎症性肠病(pediatric inflammatory bowel disease,PIBD)的发病率逐年增加,该类疾病反复发作、治疗无效率且费用昂贵。中、重度结肠炎的发病年龄较PIBD普遍偏低,且发病率大幅高于PIBD,但目前仍不清楚儿童期结肠炎是否是导致PIBD及成人炎症性肠病的风险因素。
文章作者团队发现PIBD患儿外周血血小板计数异常,应用抗血小板的传统药物双嘧达莫(商品名:潘生丁)对某些患儿有明显的治疗作用。双嘧达莫片的主要作用除了可以抑制血小板,还可以抑制磷酸二酯酶(PDE)的活性,那么从药理学的角度看,cAMP通路是必须关注的通路。
作者是在肠粘膜上皮的T细胞亚群中发现cAMP通路相关基因出现异常,从而开展解析。作者对于T细胞和NK细胞进行分群,一共又可以分为16个子亚群(下图A)。作者关注到核酸水解酶CD39(由ENTPD1编码 )在PIBD各亚型患者的CD8+和Vδ1+T细胞中表达显著降低(下图G)。CD39可以通过水解ATP、ADP为AMP,来维持免疫的稳态。
为了寻找与ENTPD1相关的基因,作者采用共表达分析的方法,发现GPR65、CD247(编码TCR zeta 链)和MAP3K8 三个关键基因与ENTPD1表达正相关。我们仔细分析一下这个3个基因中的2个。GPR65属于cAMP通路中的G蛋白偶联受体GPCR(再次注意: kegg通路每个位置都是一类分子,而一类分子下面有很多相似功能的基因)。而MAP3K8另外一个名字就是MEKK8,是我们上文讲过的MAPK通路的三级激酶系统的第一级,有活化MEK的作用。
文章中通过GWAS分析,也发现GPR65是IBD风险基因,该基因内的1个突变可以导致炎症条件下在低PH环境中cAMP浓度的降低。而其他文献报道,IBD风险突变会导致MAP3K8表达降低,这进一步确认了这两个基因值得关注。对CD8+和Vδ1+T细胞之间差异表达基因进行pathway富集分析,可以富集到cAMP-PKA和ERK (MAPK) 通路。
这里我们可以看到,作者采用了不同组学、不同分析策略,来锁定目标基因、目标通路(下图B)。这个数据整理挖掘过程,离不开对PKA通路和MAPK通路充分的了解。最终作者建立了在T细胞中,CD39的表达调控途径(下图C)。
cAMP-PKA通路和MAPK通路可以激活转录因子CREB和ATF2(都属于CREB家族)的活性,从而提高CD39的表达,进而维持免疫稳态。在患者体内,由于GPR65和MAP3K8的基因异常,导致整个通路活性不足,导致CD39表达下降,导致免疫异常、诱导肠黏膜损伤。
临床药物双嘧达莫可以通过抑制PDE,提高cAMP的浓度,从而提高PKA通路的活性,提高Navie CD8+T细胞的CD39表达,来起到治疗作用(当然,文章中作者使用了细胞实验证实了这些分析推测)。
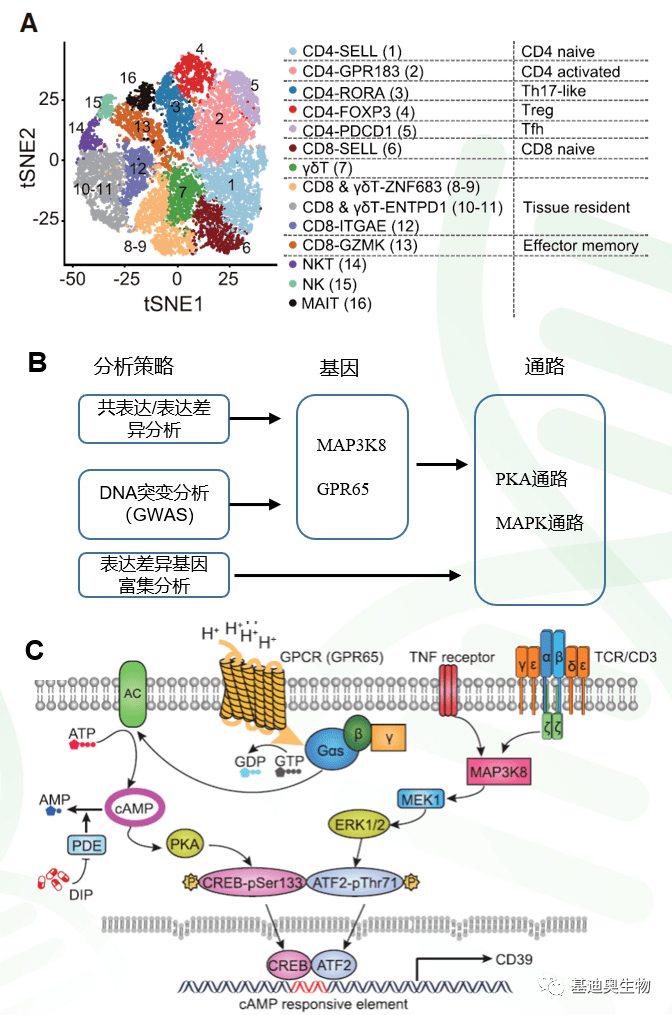
图8
总结
通过上文分析,我们会发现cAMP信号传导是细胞内作用非常广泛的通路,几乎涉及所有的生物学方向。cAMP通路的上游部分相对简单,相应的也可以作为靶向治疗的靶点。通常,细胞内cAMP的水平是主要由AC和PDE两种酶活性的平衡来调节的, 对激素和神经递质做出应答。
cAMP通路的下游部分影响的组织、细胞类型则非常广泛,影响的疾病类型也多种多样。例如,cAMP信号参与控制极化上皮细胞的胞外活动,可能与高血压、胃溃疡、甲状腺疾病、糖尿病和哮喘有关。
cAMP信号的调节有助于生理过程的形成过程,如昼夜节律的定时、性行为和神经递质串扰,信号异常也会导致神经系统疾病,如药物滥用和药物引起的运动障碍。此外,可溶性AC(ADCY10)调节的精子细胞中的cAMP通路,还可以作为男性避孕药的开发的靶点。
如果你觉得kegg系列的文章内容不错,想收看视频版的解读,也可以关注基迪奥公司旗下Omicshare在线视频课堂的专题板块《和周老师一起学KEGG通路》。在这个板块,我们会陆续与微信文章同步更新对各个通路的解读课程。
电脑端视频课程地址:
https://www.omicshare.com/class/home/index/series?id=72
另外,如果你想自己完成kegg注释,kegg富集分析等经典生物信息分析,也可以使用基迪奥公司开发的在线分析小工具Omicshare tools即可完成。使用这些在线工具,不需要任何编程基础,就可以完成专业的kegg分析工作。在这个平台上百个小工具里,kegg相关的工具也是最受用户喜欢的工具。
在线工具地址:
https://www.omicshare.com/tools/
参考文献:
[1]https://wenku.baidu.com/view/4fef8429b4daa58da0114ad6.html
[2] https://www.genecards.org
[3] Sassone-Corsi, Paolo. "The cyclic AMP pathway." Cold Spring Harbor perspectives in biology 4.12 (2012): a011148.
[4] Huang B, Chen Z, Geng L, et al. Mucosal Profiling of Pediatric-Onset Colitis and IBD Reveals Common Pathogenics and Therapeutic Pathways. Cell. 2019;179(5):1160‐1176.e24. doi:10.1016/j.cell.2019.10.027
实用科研工具推荐
详实生信软件教程分享
前沿创新组学文章解读
独家生信视频教程发布 返回搜狐,查看更多
责任编辑: