一种基于流式荧光技术的肺炎支原体IgM和IgG的同步检测方法
一种基于流式荧光技术的肺炎支原体igm和igg的同步检测方法
技术领域
1.本发明涉及一种检测方法,更具体一点说,涉及一种基于流式荧光技术的肺炎支原体igm和igg的同步检测方法,属于生物技术检测领域。
背景技术:
2.肺炎支原体(mp)是引起人类肺炎支原体肺炎的病原体。临床研究指出,mp主要经飞沫传播,各年龄段人群均可感染,在儿童及青少年中感染率较高,其与间质性肺炎、支气管肺炎等的发生都有密切联系。因此,早期诊断、早期治疗尤为重要。近年来,肺炎支原体特异性抗体mp-igm和mp-igg的检测新方法应用于临床,为临床诊断肺炎支原体感染提供了一种血清学诊断手段。
3.由于健康人血清中一般不存在mp抗体,故血清中肺炎支原体抗体igm和igg检测特异性高。应用血清学方法检测肺炎支原体的抗体igm和igg诊断呼吸道肺炎支原体感染,其抗体阳性结果能为肺炎支原体感染提供可靠的实验学依据。mp-igm一般在感染后一周内产生,第3-4周达到高峰后逐渐减弱,持续时间短;mp-igg在两周之后逐渐升高,并维持较长时间的高水平。igm和igg联合检测、联合分析、综合了igm的早期诊断优势和igg特异性强、持续时间长的优点,减少了漏诊、误诊的概率,提高了诊断正确率。在同一样品中同时完成两种抗体的检测,可降低试剂和人工的成本,且结果更可靠,具有较高的临床应用价值,应用前景广阔。
4.流式微球技术利用球形基质作为载体,以流式细胞术作为检测平台,可以在较短时间内对生物分子进行大规模检测。该系统主要基于流式荧光编码微球,检测通量大、灵敏度高,可实现同步检测多靶标,具有较为广阔的应用空间。
技术实现要素:
5.本发明提供了一种基于流式荧光技术的肺炎支原体igm和igg的检测方法,利用不同荧光编码磁性微球和同一种荧光蛋白实现在同一份样品中同时检测肺炎支原体igm和igg。
6.为了实现上述目的,本发明是通过以下技术方案实现的:
7.一种基于流式荧光技术的肺炎支原体igm和igg的同步检测方法,该制备方法为:首先,将抗人igm抗体和抗人igg抗体分别包被在不同荧光编码磁性微球表面,形成微球-igm/g抗体复合物;其次,将微球-igm/g抗体复合物与待测样品孵育,洗涤去除待测样品中的未结合成分,形成微球-igm/g抗体-igm/g复合物;再次,加入生物素标记的mp抗原和链霉亲和素标记的藻红蛋白,形成微球-igm/g抗体-igm/g-mp抗原复合物;最后,经仪器检测荧光信号强度完成检测。
8.优选的,将抗人igm抗体和抗人igg抗体分别包被在不同荧光编码磁性微球表面的包被比例为:20μg抗体包被5
×
106个荧光编码磁性微球,抗体与荧光编码磁性微球的孵育
条件为室温避光震荡1.5h。
9.优选的,形成微球-igm/g抗体复合物后,利用离心管和磁力架对编码荧光微球进行洗涤和分离,去除未结合抗体。
10.优选的,荧光编码磁性微球为固相载体,其为具有羧基基团的磁性聚苯乙烯荧光编码微球,抗人igm抗体和抗人igg抗体分别共价偶联于不同荧光编码磁性微球表面,抗体偶联微球分别与待测样本、生物素标记的mp抗原、链霉亲和素标记的藻红蛋白特异性结合,最终形成荧光免疫复合体,根据微球荧光类型和荧光强度进行检测分析。
11.优选的,利用抗人igm/g抗体、mp-igm/g、生物素标记的mp抗原、链霉亲和素标记的藻红蛋白,偶联了抗人igm抗体或抗人igg抗体的荧光微球首先与稀释的待测样品孵育,将其中igm或igg特异性结合,随后与生物素标记的mp抗原和链霉亲和素标记的藻红蛋白孵育。
12.优选的,以藻红蛋白作为荧光标记物,微球、抗人igm/g抗体、mp-igm/g和mp抗原形成免疫复合体后,根据藻红蛋白的荧光强度计算待测物含量。
13.优选的,mp抗原与藻红蛋白通过生物素-链霉亲和素系统连接。
14.优选的,利用不同荧光编码磁性微球进行编码区分,不同微球分别包被抗人igm抗体和抗人igg抗体,最终形成不同免疫复合物,用于同时检测待测样品中mp-igm和mp-igg的含量。
15.优选的,所述微球-igm/g抗体复合物是通过活化荧光微球表面的羧基,将羧基与igm/g抗体上的氨基形成共价键,从而形成复合物。
16.优选的,包括试剂盒以及放在试剂盒内的多个药剂盒,其中,具有放置不同荧光编码磁性微球的药剂盒,荧光编码微球包含有分别包被抗人igm抗体和抗人igg抗体的荧光编码微球;具有放置mp抗原溶液的药剂盒,mp抗原溶液为生物素标记mp抗原溶液,具有放置藻红蛋白的药剂盒,藻红蛋白为链霉亲和素标记藻红蛋白,具有放置标准品溶液的药剂盒,准品溶液为mp-igg和mp-igm标准品溶液,具有放置缓冲液的药剂盒,所述缓冲液为ph7.4的pbs缓冲液,试剂盒里设有可发性聚苯乙烯泡沫层,试剂盒包括盒体与盒盖,盒体与盒盖由酚醛塑料材质的连接轴连接,试剂盒底部预制有存放碎冰的冰槽。
17.有益效果:本发明可以同时检测待测样品中mp-igg和mp-igm含量,效率高、特异性强、灵敏度高、重复性好,可在临床检测、流行病学调查等方面发挥重要作用;试剂盒使用可发性聚苯乙烯泡沫材质,盒体与盒盖由酚醛塑料材质的连接轴连接,试剂盒底部预制有存放碎冰的冰槽。
附图说明
18.图1是本发明mp-igm检测标准曲线图。
19.图2是本发明mp-igg检测标准曲线图。
具体实施方式
20.以下结合说明书附图1-2,对本发明作进一步说明,但本发明并不局限于以下实施例。
21.为使本发明的目的、方法及优点更加清楚明确,下面结合具体实施例对本发明做
出详细说明。
22.本发明一种基于流式荧光技术的肺炎支原体igm和igg的同步检测方法的技术方案如下:
23.首先,将抗人igm抗体和抗人igg抗体分别包被在不同荧光编码磁性微球表面,形成微球-igm/g抗体复合物,20μg抗体包被5
×
106个磁珠,抗体与微球的孵育条件为室温避光震荡1.5h。利用离心管和磁力架对编码荧光微球进行洗涤和分离,去除未结合抗体。其次,将微球-igm/g抗体复合物与待测样品孵育,孵育条件为避光、37℃震荡1h,洗涤去除待测样品中的未结合成分,形成微球-igm/g抗体-igm/g复合物。再次,加入生物素标记的mp抗原和链霉亲和素标记的藻红蛋白,孵育条件为避光、37℃震荡1h,形成微球-igm/g抗体-igm/g-mp抗原复合物,经仪器检测荧光信号强度完成检测。
24.所述包被抗体是指抗人igm单克隆抗体和抗人igg单克隆抗体。所述微球-igm/g抗体复合物,是通过活化荧光微球表面的羧基[利用1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(edc)和n-羟基硫代琥珀酰亚胺(nhs)],将其与igm/g抗体上的氨基形成共价键,从而形成复合物。所述的微球-igm/g抗体-igm/g-连接藻红蛋白的mp抗原免疫复合物以及之前各步骤中形成的免疫复合物是指在每步孵育完成后利用离心和磁力架去除未结合成分后的物质。所述样品制备过程中的离心管和磁力架,可用酶标板和96孔板磁力架替代。所述荧光检测分析是指利用检测仪器发射的两束不同波长激发光照射免疫复合体,由荧光编码微球的荧光类型确定检测指标类型、由藻红蛋白的荧光强度确定检测指标含量。检测仪器优选tesmi f4000全自动流式荧光发光免疫分析仪。磁性微球优选美国luminex生产。
[0025]
实施例1微球-人igm抗体偶联
[0026]5×
106个微球为一个批次,将其加入至1.5ml离心管中,依次加入edc和nhs溶液,在室温、酸性条件下活化微球表面30min,随后利用磁力架将微球置换至mes缓冲液中,加入30μg抗体,室温避光震荡1.5h,利用磁力架去除未过量的抗体,加入1%bsa,室温避光震荡30h以封闭未结合位点。
[0027]
实施例2制备生物素标记mp抗原
[0028]
1mgmp抗原加入超滤管中,加入pbs缓冲液至0.5ml,12000g离心10min,超滤两次,置换缓冲体系。加入13.3μlnh2-reactive biotin及适量pbs,使蛋白浓度达到2mg/ml,37℃避光孵育0.5h。超速离心,去除未结合生物素。
[0029]
实施例3包被igm抗体微球-igm-mp抗原-藻红蛋白免疫复合物形成
[0030]
1.5ml离心管中加入微球-人igm抗体偶联物,加入待测样品溶液,37℃避光震荡1h,利用磁力架将微球用pbs洗涤2次,加入生物素标记的mp抗原和链霉亲和素标记的藻红蛋白,得到微球-igm抗体-igm抗原-藻红蛋白荧光免疫复合物,并上机检测。
[0031]
实施例4mp-igm、mp-igg检测的线性范围、灵敏度、特异性及精密度
[0032]
分别制备mp-igm和mp-igg标准品,利用本试剂盒进行检测,绘制标准曲线,利用荧光值和浓度值绘制标准曲线,mp-igm线性方程为:y=1028.4x+2174.2,r2=0.9989,线性范围为1u/ml~200u/ml,mp-igg线性方程为:y=691.15x+4092.8,r2=0.9988,线性范围为1u/ml~300u/ml,结果图1所示。
[0033]
平行测定10次0u/ml参考标准品的荧光值,并计算其均值(mean)及标准差(sd),采用mean+2sd代入标准曲线方程,计算得到本试剂盒对mp-igm的检测灵敏度为0.34u/ml,对
mp-igg的检测灵敏度为0.47u/ml。
[0034]
使用试剂盒同步检测mp-igm、mp-igg标准品,以及0.5muhbsab、5ncu/mlhbeab,hbsab和hbeab结果均为阴性,结果表明本试剂盒与hbsab、hbeab无交差反应。
[0035]
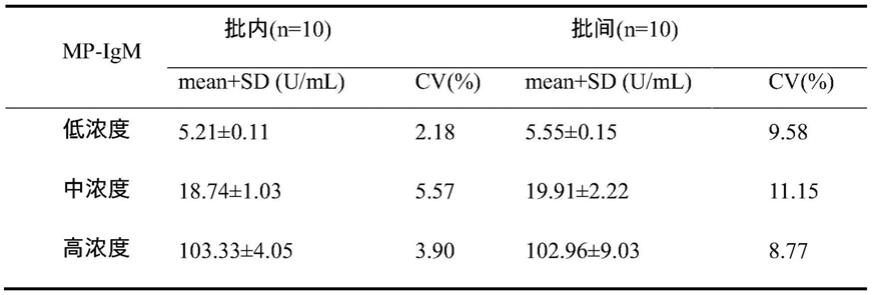
分别检测mp-igm和mp-igg的低值样本、中值样本、高值样本各10次,得到mp-igm批内变异系数为2.18%-5.57%(<10%),批间变异系数为8.77%-11.15%(<15%)。mp-igg批内变异系数为3.14%-6.58%(<10%),批间变异系数为8.14%-12.63%。
[0036]
表1 mp-igm检测精密度
[0037][0038]
表2 mp-igg检测精密度
[0039][0040]
最后,需要注意的是,本发明不限于以上实施例,还可以有很多变形。本领域的普通技术人员能从本发明公开的内容中直接导出或联想到的所有变形,均应认为是本发明的保护范围。所述的实施例只用于说明本发明,而不是用于对本发明进行限定,任何在本发明基础上所做的修改、等同替换等也均在本发明的保护范围内。
- 一种检测圆周面上V形槽位置度...
- 一种用于汽车悬架的检测装置的...
- 一种集成压力传感器和湿度传感...
- 扭转型3DMEMS探针的制作...
- 一种燃料电池金属双极板涂层耐...
- 一种用于氢氧同位素分析的土壤...
- 一种建筑面平整度检测装置的制...
- 一种槽车内低温液体纯度分析系...
- 信号测试装置、方法、计算机设...
- 红外传感器的性能测试方法、装...
- 还没有人留言评论。精彩留言会获得点赞!