有机化学学习笔记——醚
醚
2021年12月13日修改
内容如果出现错误,欢迎大家在评论区或者私信我交流改正哦。
(本文,包括之前内容如果有修改或者添加内容,会进行标注。
之前的文章同样会持续更新修改,补充一些内容。)

相信大家在很多的警匪片,犯罪片,推理片中看到过这样的情节。
一个歹徒拿着一个湿毛巾把一个受害者给迷晕。那这种看起来很可怕的迷魂剂是什么呢?
这就是今天要介绍的内容的一个典型物质——乙醚。它曾被用来作麻醉药。至于它的作用原理一些其他附加知识,这里有一个链接。
醚在有机化学书中,很多时候是和醇和酚并列出现的,比如邢大本里面,醇和醚是一个章节,李艳梅老师版本的有机化学里,醇酚醚是放在一个章节。因为醚可以看作是醇或酚的羟基中的氢被烃基取代的产物,但是醚的性质比较稳定,它在中性、碱性和弱酸性条件下稳定,常用作溶剂。
这里写错了一个知识点,石油醚主要是戊烷和己烷,虽然叫醚,但并非是真的醚。
当然,参考很多的教材,还是打算把醚中的环醚和冠醚会分开来整理,它们具有一些独特的性质,需要单独列出来讲。
专栏目录入口
结构和物理性质
结构示意
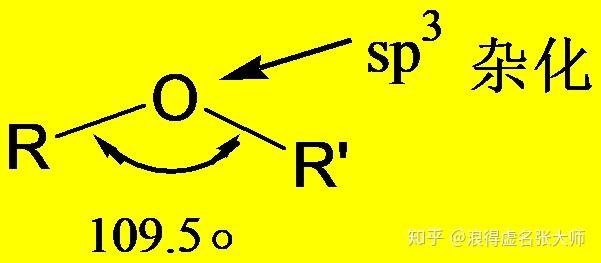

命名
注意分类
物理性质
除甲醚和甲乙醚外,其余大多数醚是无色,有特殊气味的液体,相对密度小于1。
醚比相应的异构体醇的沸点低得多,很容易挥发。
这是因为醚分子中没有羟基,不存在分子间氢键。
需要注意,醚与水分子能形成氢键,它在水中的溶解度与相应的醇差不多。
乙醚只能微溶于水,而多数的有机物易溶于乙醚,故常用乙醚从水溶液中提取易溶于乙醚的物质。
部分常见醚的物理性质——来源《有机化学 李艳梅版》

化学性质
总结
醚是一类不活泼的化合物,对碱、氧化剂、还原剂都十分稳定。
醚在常温下与金属Na不起反应,可以用金属Na来干燥。
醚的稳定性仅次于烷烃。
但其稳定性是相对的,由于醚键(C-O-C)的存在,它又可以发生一些特有的反应。

一 碱性—形成烊盐
因醚键上的氧原子有未共用电子对,能接受强酸中的质子,以配位键的形式结合生成烊盐。
可用于区分醚和烷烃或卤代烃。
要点:
与浓强酸室温或低温时形成烊盐。
醚能溶于浓强酸中。
它是一种弱碱强酸盐,仅在浓酸中才稳定,遇水很快分解为原来的醚。

- 醚与Lewis酸作用

二醚键的断裂
开始总结部分已经说过,醚键很稳定,但是稳定永远是个相对概念,也是我们需要在化学学习中需要不断给自己强调的一个概念——稳定是有条件的。
醚和氢卤酸一起加热时会发生断裂,生成醇和卤代烷。


反应活性:HI>HBr>HCl
HI常用于断裂醚键,HBr需要浓酸和较高的反应温度,HCl断裂醚键效果较差。
伯烷基醚按SN2机制断裂
叔烷基醚按SN1机制断裂
芳基烷基醚总是烷氧键断裂
乙烯基醚总是生成烯醇,然后转化成醛或酮
- SN2


- SN1


三自动氧化:过氧化物的生成
许多烷基醚与空气接触或经光照后,α位上的H会慢慢氧化,生成不易挥发的过氧化物。

过氧化物不稳定,加热时易分解而发生爆炸,因此,醚类应尽量避免暴露在空气中,一般应放在棕色玻璃瓶中,避光保存。蒸馏放置过久的乙醚时,要先检验是否有过氧化物存在,且不要蒸干。
检验方法:硫酸亚铁和硫氰化钾混合液与醚振摇,有过氧化物则显红色。

- 除去过氧化物的方法:
(1)加入还原剂5%的FeSO4于醚中振摇后蒸馏。
(2)贮藏时在醚中加入少许金属钠。
反应机理:自由基机理
- 链引发

- 链增长

四Claisen重排
苯基烯丙基醚及其类似物在加热条件下发生分子内重排,生成烯丙基酚,称为Claisen重排。
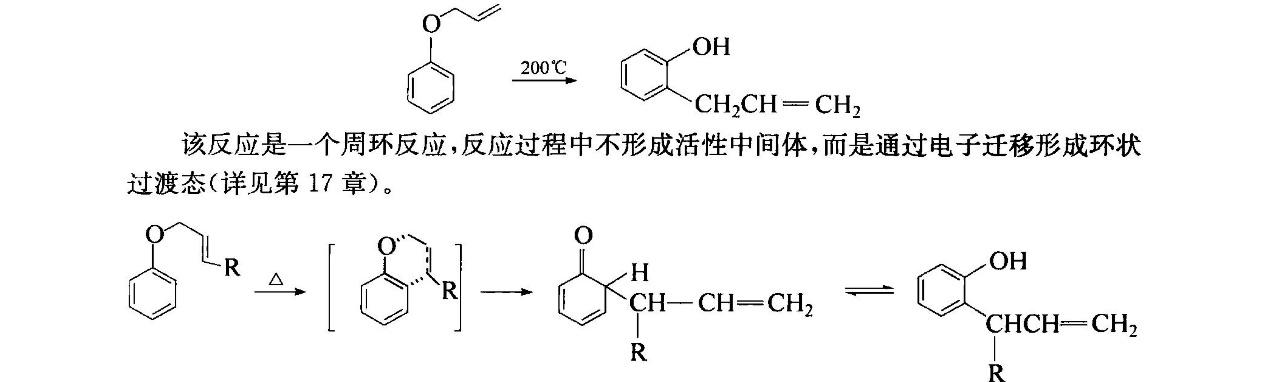
若苯基烯丙基醚的两个邻位已有取代基,则烷基可前移到对位。
醚的制备
- 醇脱水
此法只适用于制简单醚,且限于伯醇,仲醇产量低,叔醇在酸性条件下主要生成烯烃。

从原则上讲,醇在浓H2SO4作用下可以制得对称的醚。
实际上,1级ROH制醚产率好, 2级ROH制醚产率不好,3级ROH无法分离得到醚,如果蒸馏,最后得到烯。

- 威廉姆逊合成法(A.W.Williamson):由卤代烃与醇钠或酚钠作用

不能用叔卤代烷,以减少消除;
芳基烷基醚的合成总是用酚钠。
- 醇与烯烃的加成
烯烃与醇反应制备叔烷基醚——合成上的应用:保护醇羟基

例子

烯烃的烷氧汞化 —— 还原(脱汞)反应

炔烃的烷氧汞化 —— 还原反应制备烯基醚

反应遵循马氏规则:氢加在含氢较多的碳上,烷氧基加在含氢较少的碳上。
特点:不会发生消除,比威廉森合成法的限制小。
例子

环醚和冠醚
- 环醚
环氧乙烷是最简单的环醚。与一般的醚不同,环氧化合物分子中由于存在有张力的三元环,性质非常活泼,在酸碱的催化下可以与某些亲核试剂(如醇,氨,酸和格式试剂等)反应,导致环氧环打开。

- 酸催化开环:亲核试剂进攻取代较多的环氧烷碳原子

不对称环氧化合物:亲核试剂进攻能生成较稳定的碳正离子,即烃基取代基较多的碳原子;
立体化学:若被进攻的环碳原子是手性碳,则构型转化。
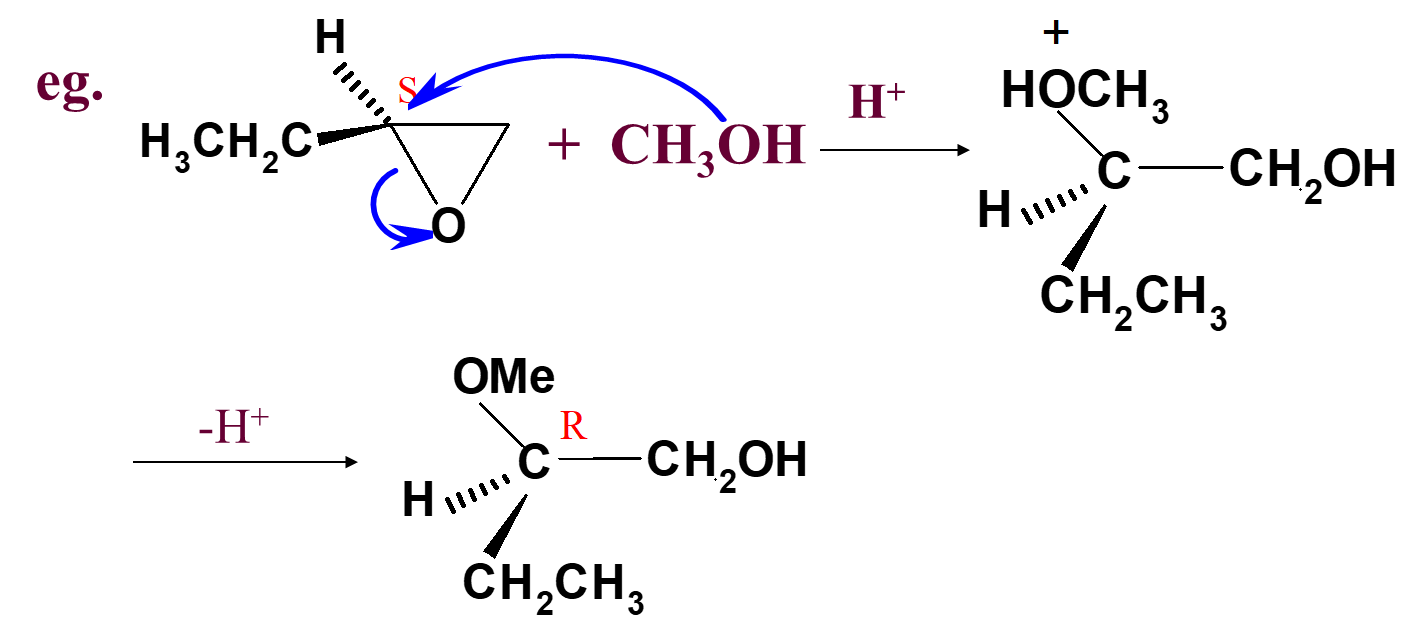
- 碱催化开环:
亲核试剂进攻取代较少的环氧烷碳原子

反应特点:碱作为Nu-从氧环背后进攻,断键与成键同时进行,为SN2反应。对于不对称环氧化合物,试剂选择进攻取代基较少(即位阻较小)的环碳原子。

立体化学:若被亲核试剂进攻的碳原子为手性碳原子,则构型转化。
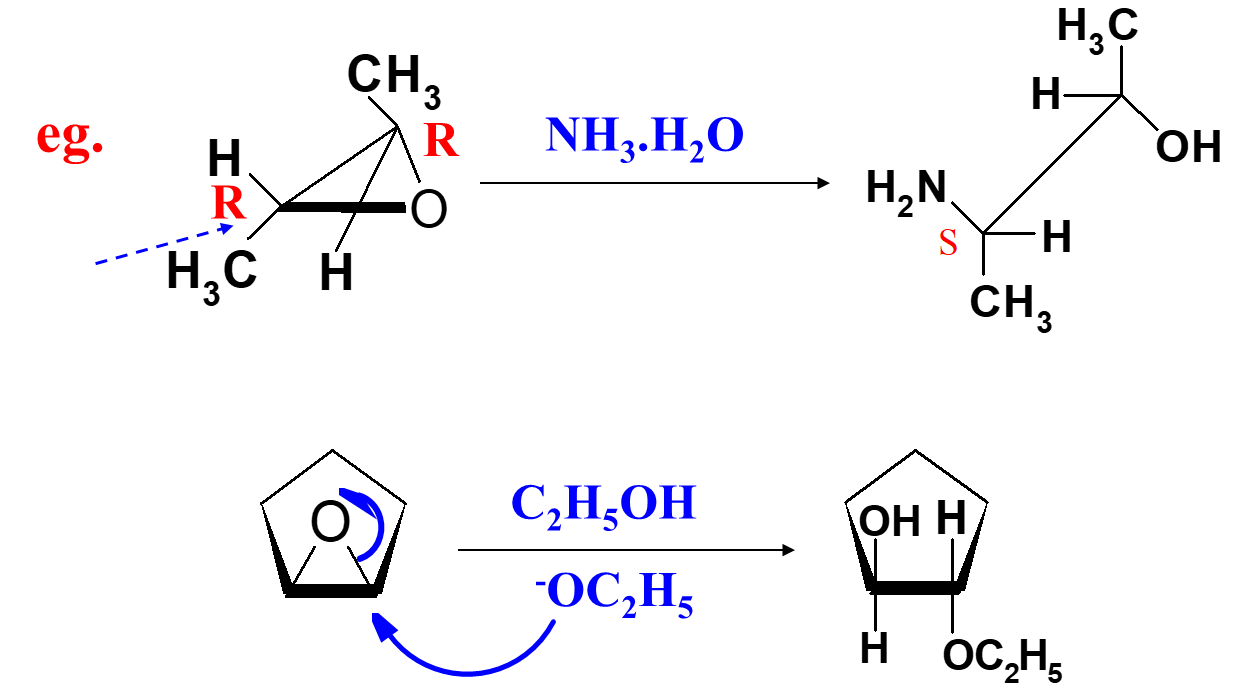
环醚反应整理

- 冠醚(Grown Ethers):为大环多醚。
结构特征是分子中具有(-OCH2CH2)n重复单位,命名:X--冠—Y,X表示环上原子总数,Y表示氧原子总数。

- 络合反应
冠醚具有特殊的大环孔状结构,在冠醚中处于环内侧的氧原子由于具有未共用电子对,可以与金属离子形成配位键,且不同结构的冠醚其分子的空穴大小不同,因此对金属离子具有较高的络合选择性。

- 相转移剂
同时,由于冠醚分子中具有亲油性的亚甲基排列在环的外侧,因而可以使盐溶于有机溶剂,或者使其从水相转移至有机相,在有机合成中常将冠醚作为相转移剂,使用非均相反应得以顺利进行,并提高收率。
不过,冠醚的价格昂贵,且毒性较大,使用后难回收,其应用受到一定程度限制。


- 冠醚的合成
Cram和Lehn获得1987年诺贝尔化学奖

文章被以下专栏收录


