如何在NMPA官网找到你想要的信息

药物临床试验从业的CRA/CRC看过来~
“ 走过路过的你,真的有认真看过NMPA的官网吗”
全文共约1500字,预计阅读时间5分钟。【多图预警】
中华人民共和国国家药品监督管理局(以下简称国家药监局)是国家市场监督管理总局管理的国家局,国家药监局作为一个体系完善的副部级司局,官网上的信息涵盖药械化安全管理、标准制定、注册管理、质量管理、上市后风险管理、执业药师管理、监督检查、对外交流合作等多项内容,本文仅介绍在注册类药物临床试验临床运营的角度去搜集相关信息的方法。本篇文章主要对以下单位进行介绍:国家药品监督管理总局(01 NMPA)、国家药品监督管理局药品审评中心(02 CDE)、国家药品监督管理局食品药品审核查验中心(03 CFDI)、国家药品监督管理局高级研修学院(04 NMPA IED)。
http://qr17.cn/Ab5XGn (二维码自动识别)
01
—
NMPA
National Medical Products Administration
https://www.nmpa.gov.cn/

查询药物临床试验机构名单2019年12月1日至2020年11月30日期间,此前已经国家药品监督管理部门会同国家卫生健康主管部门资格认定的药物临床试验机构应当通过备案系统完成备案,药物临床试验申办者仍可继续选择相应药物临床试验机构开展临床试验。自2020年12月1日起,申办者应当选取已经在备案系统备案的药物临床试验机构开展药物临床试验。在备案系统完成备案的医疗机构、疾控机构方可开展临床试验。查询中国上市药品目录集2017年12月28日国家药监局发布2017年第172号公告,发布《中国上市药品目录集》,其是国家食品药品监督管理总局发布批准上市药品信息的载体,收录批准上市的创新药、改良型新药、化学药品新注册分类的仿制药以及通过质量和疗效一致性评价药品的具体信息。指定仿制药的参比制剂和标准制剂,标示可以替代原研药品的具体仿制药品种等,供制药行业和医学界人员及社会公众了解和查询。

查询药物临床试验机构名单2019年12月1日至2020年11月30日期间,此前已经国家药品监督管理部门会同国家卫生健康主管部门资格认定的药物临床试验机构应当通过备案系统完成备案,药物临床试验申办者仍可继续选择相应药物临床试验机构开展临床试验。自2020年12月1日起,申办者应当选取已经在备案系统备案的药物临床试验机构开展药物临床试验。在备案系统完成备案的医疗机构、疾控机构方可开展临床试验。查询中国上市药品目录集2017年12月28日国家药监局发布2017年第172号公告,发布《中国上市药品目录集》,其是国家食品药品监督管理总局发布批准上市药品信息的载体,收录批准上市的创新药、改良型新药、化学药品新注册分类的仿制药以及通过质量和疗效一致性评价药品的具体信息。指定仿制药的参比制剂和标准制剂,标示可以替代原研药品的具体仿制药品种等,供制药行业和医学界人员及社会公众了解和查询。 查询药物临床试验机构名单2019年12月1日至2020年11月30日期间,此前已经国家药品监督管理部门会同国家卫生健康主管部门资格认定的药物临床试验机构应当通过备案系统完成备案,药物临床试验申办者仍可继续选择相应药物临床试验机构开展临床试验。自2020年12月1日起,申办者应当选取已经在备案系统备案的药物临床试验机构开展药物临床试验。在备案系统完成备案的医疗机构、疾控机构方可开展临床试验。查询中国上市药品目录集2017年12月28日国家药监局发布2017年第172号公告,发布《中国上市药品目录集》,其是国家食品药品监督管理总局发布批准上市药品信息的载体,收录批准上市的创新药、改良型新药、化学药品新注册分类的仿制药以及通过质量和疗效一致性评价药品的具体信息。指定仿制药的参比制剂和标准制剂,标示可以替代原研药品的具体仿制药品种等,供制药行业和医学界人员及社会公众了解和查询。

查询药物临床试验机构名单2019年12月1日至2020年11月30日期间,此前已经国家药品监督管理部门会同国家卫生健康主管部门资格认定的药物临床试验机构应当通过备案系统完成备案,药物临床试验申办者仍可继续选择相应药物临床试验机构开展临床试验。自2020年12月1日起,申办者应当选取已经在备案系统备案的药物临床试验机构开展药物临床试验。在备案系统完成备案的医疗机构、疾控机构方可开展临床试验。查询中国上市药品目录集2017年12月28日国家药监局发布2017年第172号公告,发布《中国上市药品目录集》,其是国家食品药品监督管理总局发布批准上市药品信息的载体,收录批准上市的创新药、改良型新药、化学药品新注册分类的仿制药以及通过质量和疗效一致性评价药品的具体信息。指定仿制药的参比制剂和标准制剂,标示可以替代原研药品的具体仿制药品种等,供制药行业和医学界人员及社会公众了解和查询。 - 并且可以下载相关药物的说明书(快使劲点头表示学到了)

- 可以查询符合信息化标准的术语定义、翻译



还有基药目录、进口药品信息查询、国产药品信息查询、中药保护品种、麻精药品目录等相关信息查询。

其直属单位还有中国食品药品检定研究院、国家药典委员会国家药品监督管理局药品审评中心、国家药品监督管理局食品药品审核查验中心、国家药品监督管理局药品评价中心(国家药品不良反应监测中心)、国家药品监督管理局高级研修学院、国家药品监督管理局执业药师资格认证中心等,均可在主站进行跳转。
02
—
CDE
Center For Drug Evaluation, NMPA
http://www.cde.org.cn/
国家药品监督管理局药品审评中心是国家药品监督管理局的直属单位。

- 查询并下载CDE发布征求意见稿、技术指导原则等其他工作动态

- 查询并下载ICH指导原则的英文原文/译文

- 此处可以查询临床试验默许许可情况
2018年7月27日,国家药品监督管理局发布了《国家药品监督管理局关于调整药物临床试验审评审批程序的公告》(2018年第50号),这意味着临床试验申报60日审批制度正式落地!由“点头制”变成了“摇头制”,进入了更为高效的“摇头制”时代。

- 此处可以查询上市药品的信息(包括说明书及审评审批报告)




- 此处可以查看CDE的年度审评报告
(看看CDE辛辛苦苦的成果,在中共中央办公厅 国务院办公厅印发《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》落地执行后CDE的工作效率和审批速度都得到了大大的提高~)


此处可以查看CDE优先审评及突破性治疗的公示
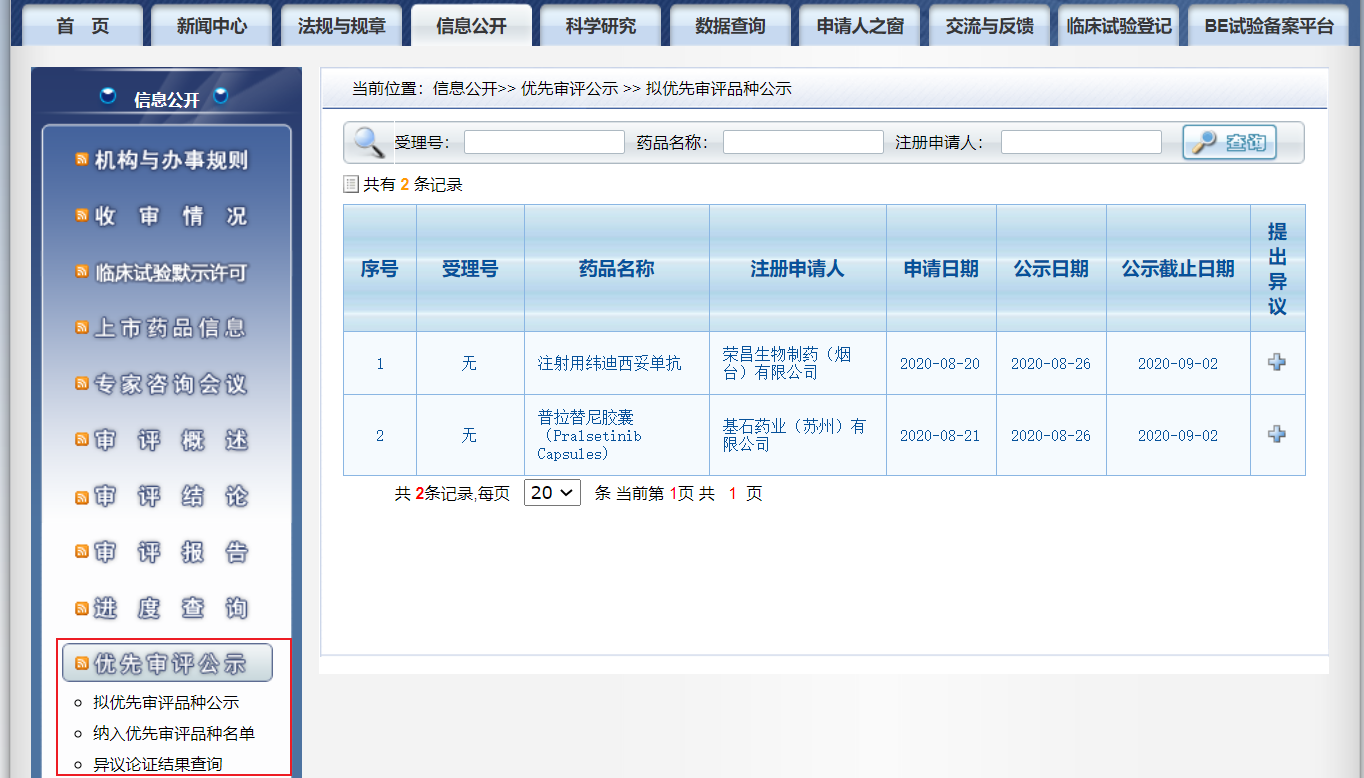
- 此处可以查看药物临床试验登记与信息公示信息
2020年7月1日发布的《药物临床试验登记与信息公示管理规范(试行)》的通告(2020年第9号)要求申办方/CRO需要定期及时在公示平台上更新相关信息,有些机构/伦理也会要求CRA提供对应项目的备案公示信息。

03
—
CFDI
Center For Food And DrugInspection Of NMPA
https://www.cfdi.org.cn/
国家药品监督管理局食品药品审核查验中心为国家药品监督管理局所属公益二类事业单位。

- 此处可以查看CFDI的政策法规

- 此处为CFDI的互动交流版块
(曾经有位机构老师需要提供新开办药企可以在没有GMP证书的情况下开展临床试验的说明,并且提到在NMPA官网上就有相关的回复,我在官网找了三个小时眼都快瞎了才找到这)

- 又是一个查询机构资质认定检查的查询入口

- 药物临床试验机构备案管理
https://beian.cfdi.org.cn/CTMDS/apps/pub/drugPublic.jsp

国家药监局 国家卫生健康委关于发布药物临床试验机构管理规定的公告(2019年第101号),药物临床试验机构由资质认定改为备案管理。国家药品监督管理局会同国家卫生健康委员会制定《药物临床试验机构管理规定》,自2019年12月1日起施行。
04
—
NMPA IED
NMPA Institute Of Executive Development
http://www.nmpaied.org.cn/

NMPA IED的培训课在行业内是有重大指导意义的,大家学习的时候可以认真的看完再去考试(毕竟考完试就不给你看了)。


