谁决定了键角的大小(价层电子对互斥理论)
NO_{2}^{+} 键角180°
NO_{2} 键角134°
NO_{2}^{-} 键角134°°
NO_{2}^{-} 和 NO_{2} 都是 sp2 杂化,其键角因为未与O成键的杂化轨道中所含孤电子数目不同而略有不同(见8月23日文“谁影响了键角的大小”)。而 NO_{2}^{+} 却是利用 sp 杂化方式成键,键角180°,分子呈直线型,与前两者相差较大。这就不仅仅是由于受到了中心原子价层电子对种类的影响,而是由价层电子对的数目不同影响了分子的空间构型导致的。
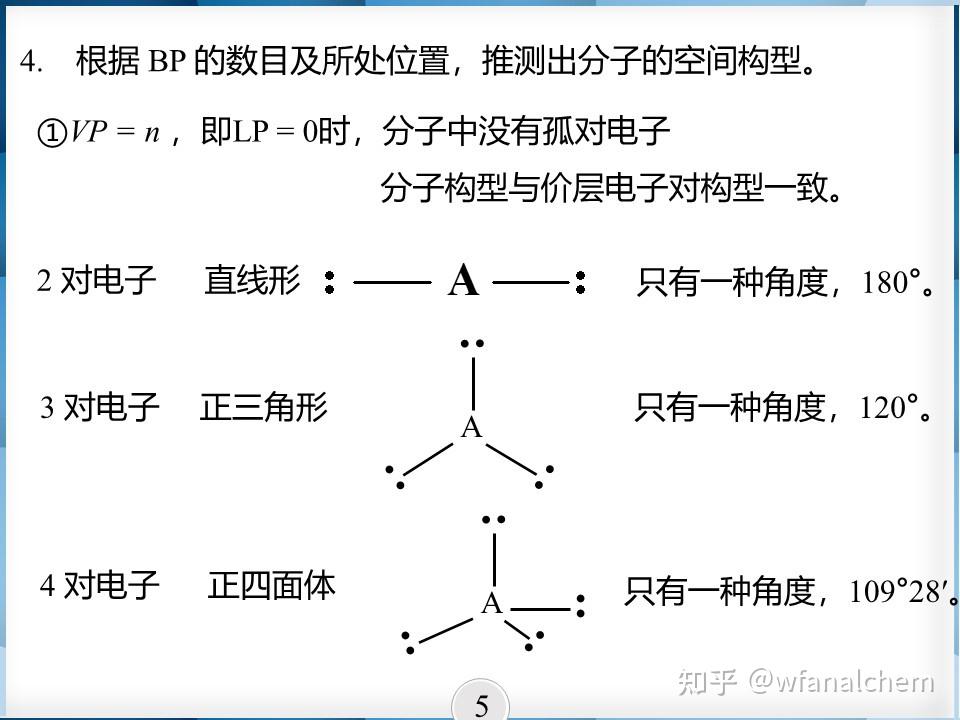
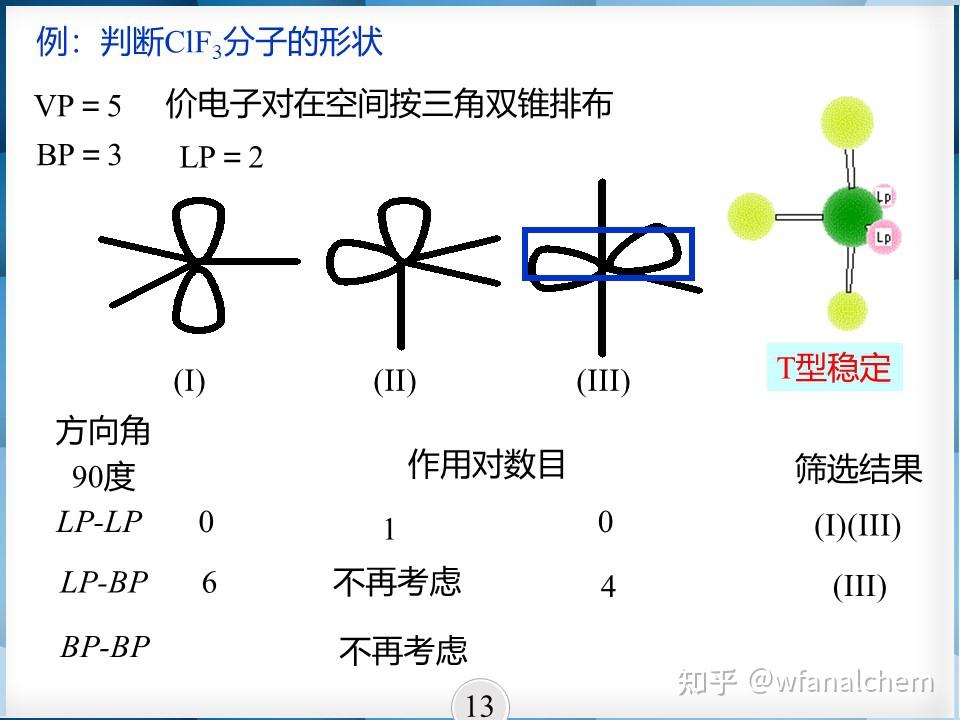
很明显,不同的空间构型,键角不同。直线型分子键角 180°,V型分子键角 <180°,平面三角型120°,正四面体109.5°,等等。
对于一个未知的主族元素化合物,我们是通过价层电子对互斥理论(VSEPR)预测和判断分子的空间构型的。
一、价层电子对互斥理论 VSEPR










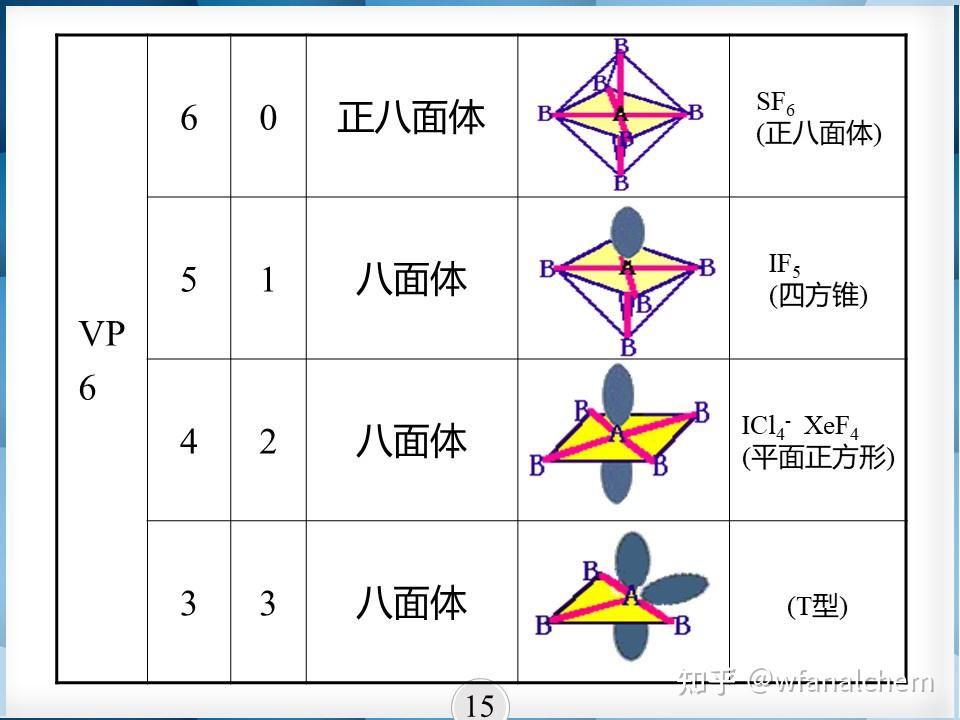
二、VSEPR与杂化轨道理论的关系
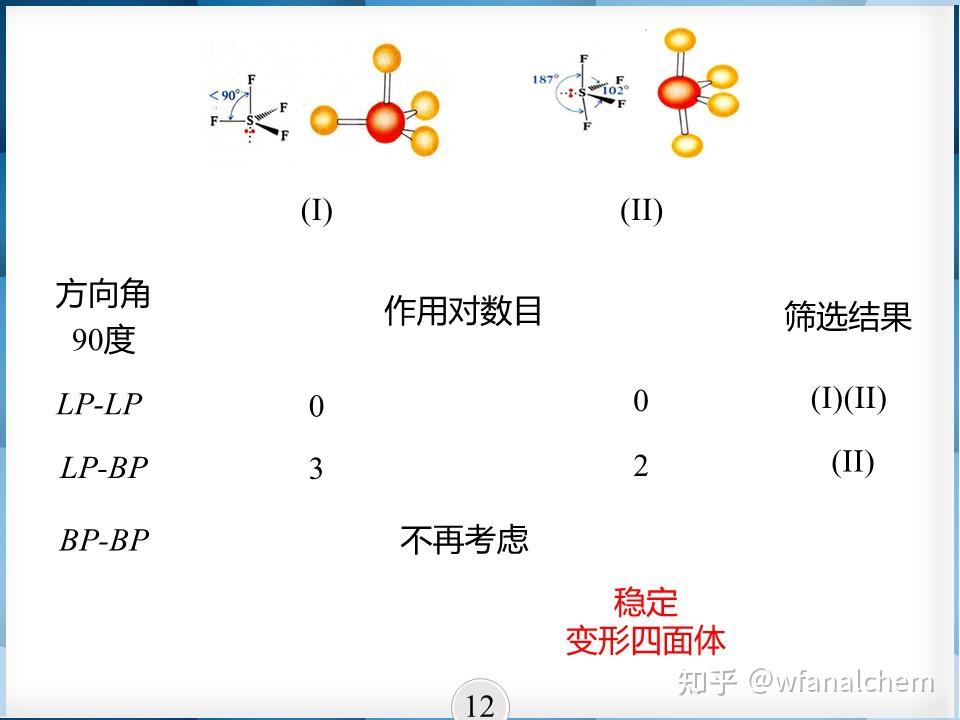
我们是基于电子对之间斥力最小的原则利用 VSEPR 预测分子的空间构型,而杂化轨道理论是基于杂化轨道在空间的排布解释经过实验测定的实际分子空间构型。一条轨道对应于一对电子(pauling不相容原理),其结论是基本一致的。
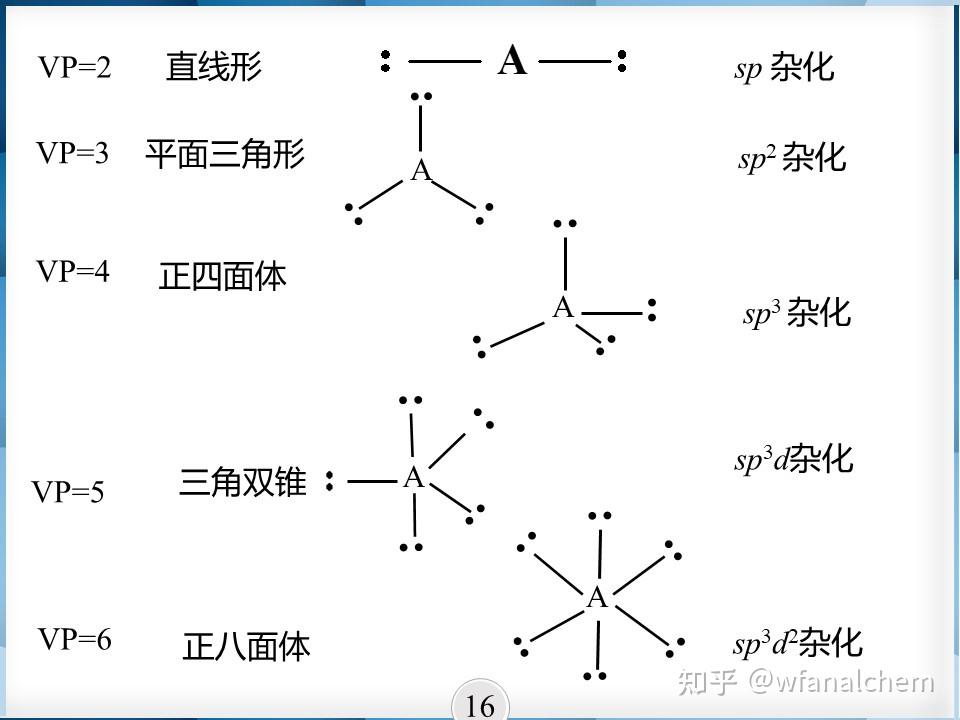
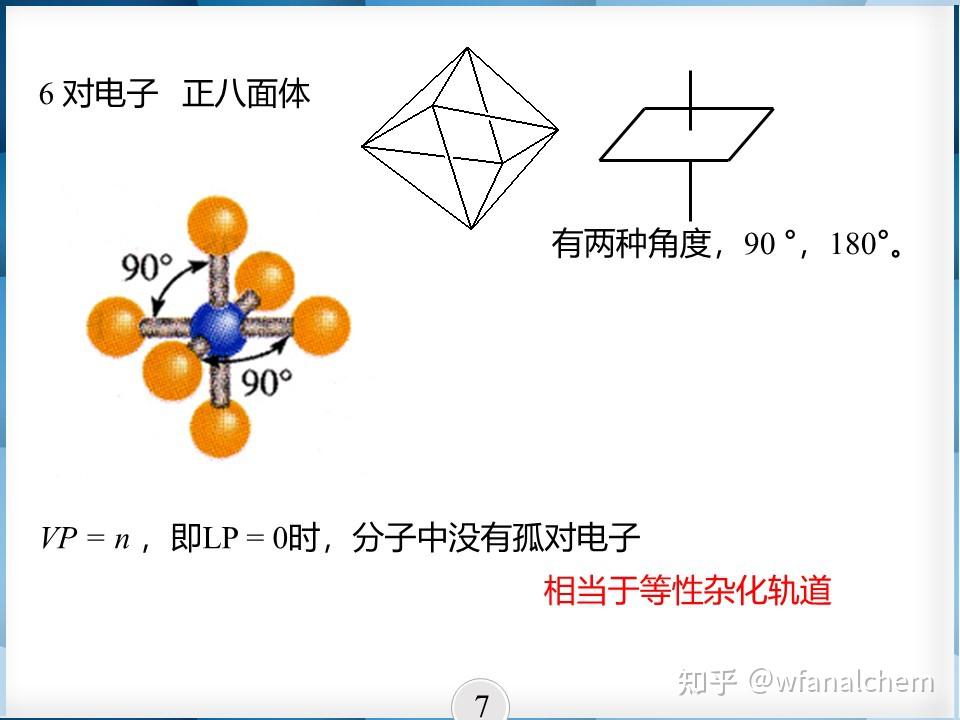
在 VSEPR 中,中心原子周围的VP全部都是成键电子对而没有孤对电子时,对应于杂化轨道理论中的等性杂化,例如 CH_{4} CH4;有孤对电子存在时,例如 NH_{3} , H_{2}O ,则对应于杂化轨道理论中的不等性杂化。
三、举一反三


四、VSEPR 的评价
1. 预测一些分子(尤其是第一、二、三周期元素组成的分子)几何构型成功而简便。
2. 对主族以外元素原子做中心原子的多原子分子构型无法预测。
3. 不涉及成键过程及键的稳定性。严格来说并不是一种化学键理论。
4. VSEPR与杂化轨道理论互为补充。

